题目内容
6.黄铜矿经初步处理后,所得溶液甲中的溶质为Fe2(SO4)3、CuSO4及H2SO4.某同学通过废铁屑与溶液甲反应,制取补血剂原料碳酸亚铁并回收铜.主要步骤如图所示: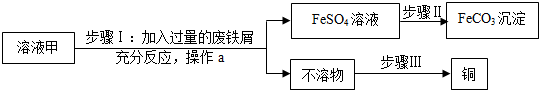
(1)Fe2(SO4)3与铁反应的化学方程式:Fe2(SO4)3+Fe=3FeSO4,该反应的基本类型为
化合反应.
(2)步骤Ⅰ中,加入过量废铁屑,观察到“有气泡放出”、“有红色固体析出”.则“有气泡放出”反应的化学方程式为:Fe+H2SO4=H2↑+FeSO4;
“有红色固体析出”反应的化学方程式为:Fe+CuSO4=Cu+FeSO4.
(3)操作a的名称是过滤,实验室进行此操作所需的玻璃仪器有烧杯、玻璃棒、漏斗.所得“不溶物”中含两种金属,其成分是铁、铜.
(4)步骤Ⅲ的目的是:除去“不溶物”中的另一种金属,回收得到纯净、干燥的铜.其操作过程为:加入过量的稀H2SO4,充分反应后再过滤并洗涤、干燥.
分析 (1)根据反应的特点分析反应的类型;
(2)根据反应的流程分析发生的反应,写出反应的化学方程式;
(3)根据过滤的原理、操作分析回答;
(4)根据混合物的成分及性质分析回答.
解答 解:(1)在Fe2(SO4)3+Fe=3FeSO4中,由两种物质生成了一种物质,属于基本类型的化合反应.
(2)由题意可知,观察到“有气泡放出”是铁与稀硫酸发生了反应,反应的化学方程式为:Fe+H2SO4=H2↑+FeSO4;观察到“有红色固体析出”是铁与硫酸铜发生了反应.反应的化学方程式为:Fe+CuSO4=Cu+FeSO4.
(3)由流程图可知,操作a是将固体与液体分离,名称是过滤,实验室进行此操作所需的玻璃仪器有烧杯、玻璃棒、漏斗.所得“不溶物”中含两种金属,其成分是剩余的铁和置换出的铜.
(4)由于铁能与稀硫酸反应生成了硫酸亚铁,铜不与硫酸反应,所以步骤Ⅲ的目的是:除去“不溶物”中的另一种金属,回收得到纯净、干燥的铜.其操作过程为:加入过量的稀H2SO4,充分反应后再过滤并洗涤、干燥.
故答为:(1)化合反应;(2)Fe+H2SO4=H2↑+FeSO4;Fe+CuSO4=Cu+FeSO4;(3)过滤,漏斗,铁、铜;(4)稀H2SO4.
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中所给的知识进行解答.

练习册系列答案
 互动英语系列答案
互动英语系列答案
相关题目
17.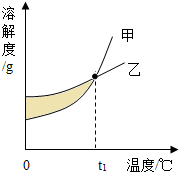 NaNO3和KNO3的溶解度数据及溶解度曲线如下,下列说法正确的是( )
NaNO3和KNO3的溶解度数据及溶解度曲线如下,下列说法正确的是( )
 NaNO3和KNO3的溶解度数据及溶解度曲线如下,下列说法正确的是( )
NaNO3和KNO3的溶解度数据及溶解度曲线如下,下列说法正确的是( ) | 温度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度S/g | NaNO3 | 87.6 | 94.9 | 110 | 122 | 148 |
| KNO3 | 31.6 | 45.3 | 85.5 | 110 | 167 | |
| A. | 30℃时,饱和溶液的溶质质量分数:NaNO3>KNO3 | |
| B. | 乙表示KNO3溶解度曲线 | |
| C. | t1℃时NaNO3和KNO3的溶解度相等,此时温度为60-80℃之间 | |
| D. | 阴影处NaNO3和KNO3的溶液均为饱和溶液 |
14.氯碱工业的反应原理是电解NaCl水溶液,下列物质不可能是氯碱工业产品的是( )
| A. | Na2C03 | B. | Cl2 | C. | H2 | D. | NaOH |
1.下列做法不符合环保理念的是( )
| A. | 提倡绿色出行,发展公共交通 | |
| B. | 减少燃煤发电,增加太阳能发电 | |
| C. | 回收利用废旧金属,保护金属资源 | |
| D. | 将高炉炼铁的废气直接排放到大气中 |
11.如图所示的基本实验操作中错误的是( )
| A. | 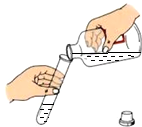 倾倒液体 | B. | 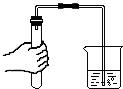 检查气密性 | C. | 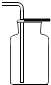 收集氢气 | D. | 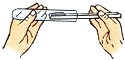 取固体药品 |
15.正常的血浆,原尿,尿液中均含有的物质是( )
①水;②无机盐;③葡萄糖;④尿素;⑤蛋白质.
①水;②无机盐;③葡萄糖;④尿素;⑤蛋白质.
| A. | ①②③ | B. | ①②④ | C. | ①③④ | D. | ①④⑤ |
16.下列各组物质中.在水中都不能溶解的-组是 ( )
| A. | MgCl2、Ca(NO3)2、BaCO3 | B. | AgCl、BaSO4、Na2CO3 | ||
| C. | AlCl3、Cu(OH)2、BaSO4 | D. | Fe(OH)3、BaCO3、AgCl |