题目内容
14.取6.4gMg和MgO的混合物,与一定量稀硫酸恰好完全反应,所得溶液中溶质的质量为24g,则原混合物中氧元素的质量为( )| A. | 1.6 g | B. | 2.56 g | C. | 3.2 g | D. | 4.8 g |
分析 镁和稀硫酸反应生成硫酸镁和氢气,氧化镁和稀硫酸反应生成硫酸镁和水,根据所得溶液中溶质硫酸镁的质量为24g,可以计算镁元素的质量,进一步可以计算原混合物中氧元素的质量.
解答 解:24g硫酸镁中,镁元素的质量为:24g×$\frac{24}{120}$×100%=4.8g,
则原混合物中氧元素的质量为:6.4g-4.8g=1.6g,
故选:A.
点评 本题主要考查学生进行计算和推断的能力,比较简单,计算时要注意规范性和准确性.

练习册系列答案
相关题目
5.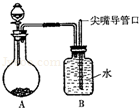 小茜设计了一个趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体不可行的是( )
小茜设计了一个趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体不可行的是( )
 小茜设计了一个趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体不可行的是( )
小茜设计了一个趣味实验装置(见图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体不可行的是( )| A. | 氧化钙和水 | B. | 硝酸铵和水 | ||
| C. | 二氧化锰和过氧化氢溶液 | D. | 锌粒和硫酸溶液 |
9.CaCO3、CuCl2溶液、KOH 溶液、Zn粒四种物质单独或相互反应,没有涉及到的基本反应类型是( )
| A. | 复分解反应 | B. | 分解反应 | C. | 置换反应 | D. | 化合反应 |
3.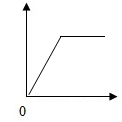 如表各选项与如图所示曲线相符的是( )
如表各选项与如图所示曲线相符的是( )
 如表各选项与如图所示曲线相符的是( )
如表各选项与如图所示曲线相符的是( )| 序号 | 横坐标 | 纵坐标 |
| A | 向一定量稀硫酸中加入锌粉的质量 | 溶液中氢元素的质量 |
| B | 向一定量的氢氧化钠和碳酸钠混合溶液中加入稀盐酸的质量 | 产生气体的质量 |
| C | 向混有盐酸的硫酸钠溶液中加入氢氧化钡溶液的质量 | 生成沉淀的质量 |
| D | 在一定温度下,向一定量不饱和硝酸钾溶液中加入硝酸钾固体的质量 | 溶液中溶质的质量分数 |
| A. | A | B. | B | C. | C | D. | D |
4.下列变化属于物理变化的是( )
| A. | 石蜡熔化 | B. | 食物腐烂 | C. | 粮食酿酒 | D. | 钢铁生锈 |