题目内容
1. 向100克盐酸和氯化铵的混合溶液中,逐滴滴入质量分数为20%的氢氧化钠溶液,搅拌使其充分反应,所加氢氧化钠溶液的质量和生成气体的质量关系如图所示.计算:(规范书写计算过程)
向100克盐酸和氯化铵的混合溶液中,逐滴滴入质量分数为20%的氢氧化钠溶液,搅拌使其充分反应,所加氢氧化钠溶液的质量和生成气体的质量关系如图所示.计算:(规范书写计算过程)(1)求参加反应的氯化氢质量;
(2)求最终产生的气体质量;
(3)当加入60g氢氧化钠溶液后,恰好反应,欲将该溶液稀释成溶质质量分数为8.775%的溶液,还应向该溶液中加入多少克水?
分析 (1)根据图象可知与稀盐酸反应的氢氧化钠溶液是20g,依据化学方程式即可解答;
(2)根据图象可知与氯化铵反应的氢氧化钠溶液是60g-20g=40g,依据化学方程式即可解答;
(3)根据化学方程式计算出所得氯化钠质量,再根据稀释溶液时溶质的质量不变列方程解答.
解答 解:(1)设参加反应的氯化氢的质量为x,同时生成氯化钠的质量为z,
HCl+NaOH=NaCl+H2O
36.5 40 58.5
x 20g×20% z
$\frac{36.5}{x}=\frac{40}{20g×20%}=\frac{58.5}{z}$
x=3.65g; z=5.85g;
(2)设最终产生的气体的质量为y,生成氯化钠质量为n,
NH4Cl+NaOH=NaCl+H2O+NH3↑
40 58.5 17
(60g-20g)×20% n y
$\frac{40}{(60g-20g)×20%}=\frac{58.5}{n}=\frac{17}{y}$
y=3.4g; n=11.7g
(3)设欲将该溶液稀释成溶质质量分数为8.775%的溶液,还应向该溶液中加水质量为m,
5.85g+11.7g=(100g+60g-3.4g+m)×8.775%
m=43.4g
答:(1)参加反应的氯化氢的质量是3.65g;
(2)最终产生的气体的质量为3.4g;
(3)欲将该溶液稀释成溶质质量分数为8.775%的溶液,还应向该溶液中加水质量为43.4g.
点评 培养学生的看图能力,能够判断反应的过程,理清反应过程各物质的质量之间的关系,注意计算的格式和规范.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.我国科学家屠呦呦因为“发现青蒿素(一种用于治疗疟疾的药物),挽救了全球特别是发展中国家的数百万人的生命”而获拉斯克奖.青蒿素是治疗疟疾的特效药,青蒿素化学式为C15H22O5.下列关于青蒿素的说法正确的是( )
| A. | 青蒿素含有42个原子 | B. | 青蒿素属于有氧化物 | ||
| C. | 青蒿素中C、H、O的质量比是15:22:5 | D. | 青蒿素中碳元素质量分数最高 |
6.通常情况下,几种物质的着火点如表
根据表中所给信息和所学相关知识判断,下列说法错误的是( )
| 物质 | 白磷 | 红磷 | 木炭 | 无烟煤 |
| 着火点/℃ | 40 | 240 | 320-370 | 700-750 |
| A. | 白磷、红磷、木材、酒精都是可燃物 | |
| B. | 降低可燃物的着火点可以达到灭火的目的 | |
| C. | 实验时,用于吸干白磷的滤纸片不能丢在废纸篓里 | |
| D. | 红磷燃烧属于置换反应 |
10.下列不属于中和反应在生产生活中的应用的是( )
| A. | 用石灰粉改良酸性土壤 | B. | 往造纸厂排放的碱溶液中加盐酸 | ||
| C. | 含氢氧化铝的胃药治疗盐酸过多 | D. | 硫酸铜与碱石灰配置波尔多液 |
11.他们取样品125g,用35%的盐酸处理,其实验数据如下:
请回答下列问题
(1)该石灰石样品中含碳酸钙的质量分数是多少;
(2)实验过程中实际参加反应的盐酸的质量是多少,(精确到0.1g).
| 实验次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 加入稀盐酸体积/mL | 40 | 40 | 40 | 40 | 40 |
| 剩余固体的质量/g | 103 | 73 | 36 | 33 | 25 |
(1)该石灰石样品中含碳酸钙的质量分数是多少;
(2)实验过程中实际参加反应的盐酸的质量是多少,(精确到0.1g).
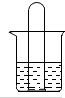 小明同学为了探究二氧化碳的性质,设计了如图所示的实验:在盛有水的烧杯中滴入紫色石蕊溶液,将一个充满二氧化碳的试管倒立在其中.
小明同学为了探究二氧化碳的性质,设计了如图所示的实验:在盛有水的烧杯中滴入紫色石蕊溶液,将一个充满二氧化碳的试管倒立在其中.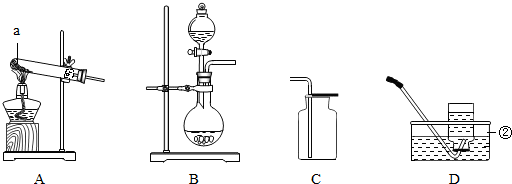
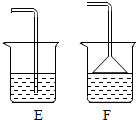
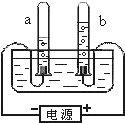 实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题:
实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题: