题目内容
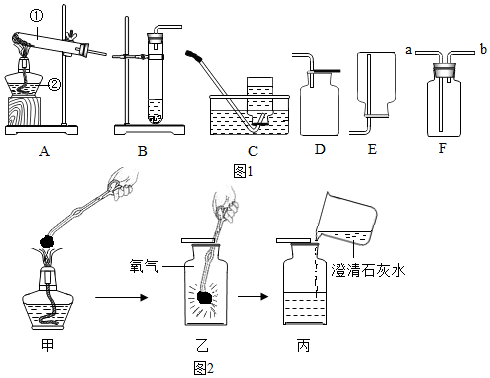
17.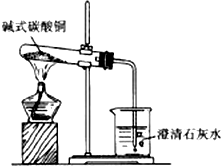 某兴趣小组为了探究碱式碳酸铜【化学式为Cu2(OH)2CO3】加热后分解的产物.取一定量样品进行加热,生成黑色固体,并产生能使澄清石灰水变浑浊的气体,思考并回答:
某兴趣小组为了探究碱式碳酸铜【化学式为Cu2(OH)2CO3】加热后分解的产物.取一定量样品进行加热,生成黑色固体,并产生能使澄清石灰水变浑浊的气体,思考并回答:(1)产生的气体中肯定含有CO2;
(2)【提出问题】该黑色固体的主要成分是什么?
【查阅资料】碱式碳酸铜分解的产物均为化合物.
【猜想与假设】①可能是炭黑(碳的单质);
②可能是铁或铁的氧化物;
③可能是氧化铜.
你认为上述猜想缺乏依据的是②(填编号),理由是根据质量守恒定律,反应前后元素种类不变、反应前后原子种类不变,反应物中没有铁元素;
(3)从上述实验现象中,你能否判断有水蒸气产生(填“能”或“不能”)不能;不用任何试剂,你判断是否有水生成的方法是用干燥的烧杯罩在导管口(或试管口),如烧杯内壁有水珠,则有水蒸气产生.
(4)【实验验证】:将试管口的无色液体收集,并连接水的电解器,通直流电一段时间后,正极与负极的气体体积比为1:2,且正极为氧气,负极为氢气,故无色液体为水.
(5)【交流讨论】根据以上内容,请写出碱式碳酸铜受热分解的化学方程式Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O.
分析 根据对Cu2(OH)2CO3样品进行加热,生成黑色固体,并产生能使澄清石灰水变浑浊的气体.则
(1)和(2)中由现象和元素守恒,气体为二氧化碳,可知黑色固体为氧化铜,
(3)在现象的描述中不能确定有水生成,需要用干燥的烧杯中是否有水来说明;
(4)结合电解水的实验分析解答;
(5)根据以上信息解答书写方程式.
解答 解:(1)因二氧化碳能使澄清石灰水变浑浊,则气体为二氧化碳,故选CO2.
(2)在碱式碳酸铜中不含有铁元素,则黑色固体肯定与铁及铁的氧化物无关,故答案为:②;根据质量守恒定律,反应前后元素种类不变、反应前后原子种类不变,反应物中没有铁元素.
(3)实验现象中不能确定是否有水生成,需利用干燥的仪器来证明有水的生成,故答案为:不能;用干燥的烧杯罩在导管口(或试管口),如烧杯内壁有水珠,则有水蒸气产生(或观察试管口有冷凝水,说明有水蒸气产生;收集产生的气体冷却有冷凝水)(其它合理的方法都可).
(4)实验现象中不能确定是否有水生成,所以将试管口的无色液体收集,通直流电,一段时间后,正极与负极的气体体积比为1:2,且正极为氧气,负极为氢气,证明该无色液体为水.故答案为:水.
(5)根据以上内容可知,碱式碳酸铜受热分解的生成物是CuO、CO2、H2O;故答案为:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O.
点评 本题以探究的方式让学生根据实验现象和质量守恒定律来分析解答,可较好的训练学生思维,提高知识的迁移使用的能力.

练习册系列答案
相关题目
9.下列化学反应中,既是化合反应又是氧化反应的是( )
| A. | 镁+氧气$\stackrel{点燃}{→}$ 氧化镁 | B. | 氧化汞 $\stackrel{加热}{→}$ 汞+氧气 | ||
| C. | 石蜡+氧气$\stackrel{点燃}{→}$ 二氧化碳+水 | D. | 水 $\stackrel{通电}{→}$ 氢气+氧气 |
12.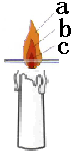 某同学对蜡烛(主要成分是石蜡)及其燃烧进行了探究.其实验步骤有:
某同学对蜡烛(主要成分是石蜡)及其燃烧进行了探究.其实验步骤有:
①点燃蜡烛,紧贴烛芯将火柴梗放入火焰中约1秒后取出
②在火焰上方罩一个冷而干燥的小烧杯; ③用火柴去点白烟;
④切下一块石蜡,放入水中;⑤熄灭蜡烛;⑥迅速倒转烧杯,加入澄清石灰水,振荡.
请回答以下问题:
(1)参看(2)的实验记录,以上操作步骤的正确排序是④①②⑥⑤③.
(2)按要求填写下列实验现象及其结论.
结论:蜡烛燃烧生成水和二氧化碳.
 某同学对蜡烛(主要成分是石蜡)及其燃烧进行了探究.其实验步骤有:
某同学对蜡烛(主要成分是石蜡)及其燃烧进行了探究.其实验步骤有:①点燃蜡烛,紧贴烛芯将火柴梗放入火焰中约1秒后取出
②在火焰上方罩一个冷而干燥的小烧杯; ③用火柴去点白烟;
④切下一块石蜡,放入水中;⑤熄灭蜡烛;⑥迅速倒转烧杯,加入澄清石灰水,振荡.
请回答以下问题:
(1)参看(2)的实验记录,以上操作步骤的正确排序是④①②⑥⑤③.
(2)按要求填写下列实验现象及其结论.
| 探究步骤 | 对实验的观察和描述 |
| 点燃前 | (1)取一支蜡烛,用小刀切下一小块,把它放入水中,蜡烛会浮于水面,难溶于水. 结论:石蜡的密度比水小. |
| 燃着时 | (2)点燃蜡烛,观察到蜡烛的火焰分为三层,分别是外焰、内焰、焰心.把一根火柴梗放在蜡烛的火焰上(如图),约1S后取出,可以看到在a处(填字母)的火柴梗的最先碳化.结论:蜡烛火焰的外焰温度最高. (3)再将一只干燥的烧杯罩在蜡烛火焰上方,烧杯内壁出现水雾,片刻后取下烧杯,迅速向烧杯内倒入少量澄清的石灰水,振荡后发现变浑浊. 结论:蜡烛燃烧以后的生成物是水和二氧化碳. |
| 熄灭后 | 吹灭蜡烛,观察到一缕白烟. |
1.下列方案的设计中,可行的是( )
①在树木上涂刷石灰浆,可保护树木;②图书馆内图书失火,选用二氧化碳灭火器扑灭;③用NaOH溶液除去CO2中的CO气体;④用溶解、过滤、蒸发的方法提纯粗盐;⑤用食品级碳酸氢钠和柠檬酸自制汽水.⑥用肥皂水区分硬水和软水.
①在树木上涂刷石灰浆,可保护树木;②图书馆内图书失火,选用二氧化碳灭火器扑灭;③用NaOH溶液除去CO2中的CO气体;④用溶解、过滤、蒸发的方法提纯粗盐;⑤用食品级碳酸氢钠和柠檬酸自制汽水.⑥用肥皂水区分硬水和软水.
| A. | ②③⑥ | B. | ②④⑤⑥ | C. | ①②④⑤⑥ | D. | ③⑤⑥ |
6.固体物质的溶解度与下列哪一个因素无关( )
| A. | 溶液温度的高低 | B. | 溶质、溶剂量的多少 | ||
| C. | 溶质的种类和性质 | D. | 溶剂的种类和性质 |
3.大理石的主要成分是碳酸钙,在探究大理石性质时,下列有关实验现象和结论的描述中,不正确的是( )
| A. | 在大理石的板砖碎片上,滴加稀盐酸有气泡产生 | |
| B. | 大理石雕像不易受酸雨侵蚀 | |
| C. | 实验室里可用大理石与稀盐酸来制取二氧化碳 | |
| D. | 大理石与酸反应生成的气体可作灭火剂 |
4.诗词是民族灿烂文化中的瑰宝.下列古诗词中一定不涉及化学变化的是( )
| A. | 日照香炉生紫烟,遥看瀑布挂前川 | B. | 春蚕到死丝方尽,蜡炬成灰泪始干 | ||
| C. | 千锤万凿出深山,烈火焚烧若等闲 | D. | 爆竹声中一岁除,春风送暖入屠苏 |