题目内容
8.今天是实验室的开放日,某小组的同学利用下列装置进行实验.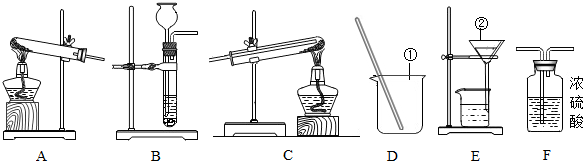
(1)写出图中指定仪器的名称:①烧杯;②漏斗.
(2)要制取干燥的H2,并用H2还原氧化铜,应选取的装置为B、F、C(填装置编号).在氢气还原氧化铜的过程中,同学们能观察到的现象是黑色固体变红色,试管口有水滴.
(3)若制取氢气时需要100g 9.8%的稀硫酸,配制上述稀硫酸需要98%的浓硫酸(密度为1.84g/cm3)5.4mL.配制过程中,除上图装置中的仪器外,还缺少的仪器有②④⑤(填序号).
①天平 ②胶头滴管 ③药匙 ④10mL量筒 ⑤100mL量筒
(4)还原氧化铜的实验结束后,同学们发现得到的铜中还混有未反应的氧化铜.为了得到纯净的铜,他们进行了以下实验操作:
| 操作 | 简答 |
| ①将反应后的固体放入烧杯中,加入足量的稀硫酸,搅拌,使其充分反应. | 加足量稀硫酸的目的是: 使氧化铜完全反应 |
| ②将操作①中所得的混合物过滤. | 滤液中所含有的溶质是: 使氧化铜完全反应 |
| ③将操作②所得的滤渣洗涤、烘干,得到纯净的铜. | / |
分析 (1)写出常见化学仪器名称;
(2)选择固液常温反应装置制氢气及干燥方法,熟悉氢气还原氧化铜的实验装置及反应现象;
(3)掌握稀释浓硫酸的方法及所需仪器,根据稀释前后容质量不变计算所需浓硫酸的质量,由密度求其体积量;
(4)熟悉一些分离混合物的方法,掌握一些硫酸的化学性质.
解答 解:(1)题干中指定的仪器名称是①烧杯、②漏斗;
(2)实验室制取氢气常用锌和稀硫酸反应,采用固液反应装置,干燥氢气常用浓硫酸,因其具吸水性,氢气还原氧化铜固体需将导气管通入试管底部氧化铜的上方加热,故应选装置B、F、C;反应时会出现黑色固体变红色,试管口有水滴生成的现象;
(3)稀释浓硫酸时,根据稀释前后容质量不变计算所需浓硫酸的质量,再由密度求其体积量,即:100g×9.8%═浓硫酸质量×98%,浓硫酸质量═10g,由密度公式求得浓硫酸体积═5.4mL,稀释浓硫酸用到烧杯、玻璃棒、胶头滴管、量筒,故缺少仪器选②④⑤.
(4)
| 操作 | 简答 |
| ①将反应后的固体放入烧杯中,加入足量的稀硫酸,搅拌,使其充分反应. | 加足量稀硫酸的目的是:使氧化铜完全反应 |
| ②将操作①所得的混合物过滤. | 滤液中所含有的溶质是:CuSO4、H2SO4 |
| ③将操作②所得的滤渣洗涤、烘干,得到纯净的铜, |
(2)B、F、C.黑色固体变红色,试管口有水滴.
(3)5.4;②④⑤.
(4)①使氧化铜完全反应;②CuSO4;H2SO4.
点评 此题考查了常用仪器的识别与书写,氢气的实验室制法、干燥方法及其还原性,有关溶液的稀释计算及配制溶液的方法、所需仪器的熟悉了解,混合物的分离等知识,涉及知识面广,能很好的培养学生的知识掌握能力.

练习册系列答案
相关题目
6.以下化学实验的基本操作正确的是( )
| A. | 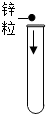 | B. | 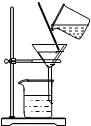 | C. | 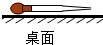 | D. | 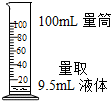 |
3.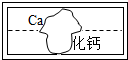 某组同学在学习盐的性质时,将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的探究.
某组同学在学习盐的性质时,将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的探究.
探究一:M溶液中的溶质是什么?
(1)【提出猜想】该组同学认为M溶液的溶质有两种可能:①是Ca(OH)2,②是CaCl2.
【收集资料】CaCl2水溶液呈中性.
(2)【设计实验】同学们设计了如下方案并进行实验:
请写出碳酸钠与溶液M反应的化学方程式Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
探究二 过滤后澄清滤液中会有哪些溶质?
【提出猜想】猜想一:NaOH 和Na2CO3;猜想二:NaOH和Ca(OH)2;猜想三:NaOH
(3)【实验验证】同学们针对“猜想一”进行了如下实验:
他们的实验结论是否正确?否,理由是加入的(少量)盐酸先与溶液中的氢氧化钠反应,即使溶液中有碳酸钠,也可能不产生气体.
(4)【继续探究】设计实验方案确定滤液中溶质的组成.
(5)【反思与拓展】在分析反应后所得溶液中溶质时,除考虑可溶性的生成物,还应考虑反应物是否有剩余.
 某组同学在学习盐的性质时,将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的探究.
某组同学在学习盐的性质时,将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液.同学们对该实验进行了一系列的探究.探究一:M溶液中的溶质是什么?
(1)【提出猜想】该组同学认为M溶液的溶质有两种可能:①是Ca(OH)2,②是CaCl2.
【收集资料】CaCl2水溶液呈中性.
(2)【设计实验】同学们设计了如下方案并进行实验:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量M溶液于试管中,向其中滴加无色酚酞试液 | 溶液变红色 | 猜想①正确. |
探究二 过滤后澄清滤液中会有哪些溶质?
【提出猜想】猜想一:NaOH 和Na2CO3;猜想二:NaOH和Ca(OH)2;猜想三:NaOH
(3)【实验验证】同学们针对“猜想一”进行了如下实验:
| 实验操作 | 实验现象 | 实验结论 |
| 取样于试管中,滴入几滴稀盐酸 | 没有气体产生 | “猜想一”不成立 |
(4)【继续探究】设计实验方案确定滤液中溶质的组成.
| 实验操作 | 实验现象 | 实验结论 |
| 分别取少量滤液于A、B两支试管中,A中加入CaCl2溶液, B中加入Na2CO3溶液 | 若A中产生白色沉淀,B中没有沉淀 | “猜想一”成立 |
| 若A中没有沉淀,B中产生白色沉淀 | “猜想二”成立 | |
| 若A、B两支试管中都没有沉淀产生 | “猜想三”成立 |
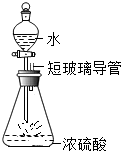 如图,在500mL锥形瓶中盛约25mL浓硫酸.将分液漏斗中的水缓慢滴人锥形瓶中.观察到的现象是水沸腾,液滴飞溅,解释产生此现象的原因是:水的密度较小,浮在浓硫酸的上面,浓硫酸溶解时放出的热会使水立刻沸腾,使液滴向四周飞溅,若堵塞短玻璃导管可能产生的后果是把瓶塞弹出或导致锥形瓶炸裂,理由是若堵塞导管,气体无法导出,膨胀的气体使瓶内气压变大,大于外界气压,把胶塞弹出或使锥形瓶炸裂.
如图,在500mL锥形瓶中盛约25mL浓硫酸.将分液漏斗中的水缓慢滴人锥形瓶中.观察到的现象是水沸腾,液滴飞溅,解释产生此现象的原因是:水的密度较小,浮在浓硫酸的上面,浓硫酸溶解时放出的热会使水立刻沸腾,使液滴向四周飞溅,若堵塞短玻璃导管可能产生的后果是把瓶塞弹出或导致锥形瓶炸裂,理由是若堵塞导管,气体无法导出,膨胀的气体使瓶内气压变大,大于外界气压,把胶塞弹出或使锥形瓶炸裂.