题目内容
2.设NA表示阿伏加德罗常数,下列叙述中正确的是( )| A. | 常温常压下,11.2L NH3所含的原子数为2NA | |
| B. | 常温常压下,80g SO3含有的氧原子数为3NA | |
| C. | 标准状况下,5.6 L四氯化碳含有的分子数为0.25NA | |
| D. | 一定条件下,56g铁粉与足量的盐酸完全反应转移电子数目为3NA |
分析 A、考虑11.2LNH3处于常温常压,不是标准状况,进行分析;
B、考虑常温常压下,48gO3含有的氧原子数为$\frac{80g}{80g/mol}×{N}_{A}mo{l}^{-1}×3$=3NA;
C、考虑标准状况下,四氯化碳不是气体;
D、考虑铁与足量的盐酸完全反应,转化为亚铁离子.
解答 解:
A、11.2LNH3处于常温常压,不是标准状况,不能使用气体摩尔体积22.4L/mol,故A错误;
B、常温常压下,48gO3含有的氧原子数为$\frac{80g}{80g/mol}×{N}_{A}mo{l}^{-1}×3$=3NA,故B正确;
C、标准状况下,四氯化碳不是气体,无法计算5.6 L四氯化碳含有的分子数,故C错误;
D、56g铁粉的物质的质量为$\frac{56g}{56g/mol}=1mol$,与足量的盐酸完全反应,铁转化为亚铁离子,则转移电子数目为2NA,故D错误.
故选B.
点评 本题主要考查常用化学计量的有关计算和理解,难度不大,注意气体摩尔体积使用条件和对象.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
1.下列气体在洁净空气中不应该含有的是( )
| A. | 氩气 | B. | 氧气 | C. | 二氧化硫 | D. | 二氧化碳 |
7.牙膏是生活中常见的物质,其配料成分有摩擦剂、增稠剂、发泡剂等,其中摩擦剂的类型有很多,如CaCO3、Al(OH)3、SiO2或这些物质的混合物.我校化学兴趣小组同学想研究牙膏摩擦剂的成分.
【实验探究一】某品牌牙膏中是否含有CaCO3?
【查阅资料】二氧化硅不与稀盐酸反应
【实验方案】
【实验探究二】该牙膏中CaCO3的含量是多少?
【实验装置】利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.
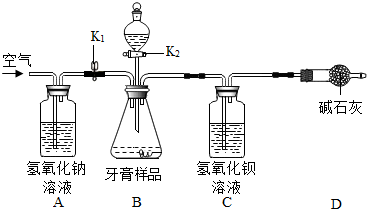
【友情提示】
(1)氢氧化钡跟氢氧化钙的性质类似,CO2+Ba(OH)2═BaCO3↓+H2O;
(2)CO2的相对分子质量为44,CaCO3的相对分子质量为100,BaCO3的相对分子质量为197;
(3)以上药品均足量,且每步反应或作用都是完全的.
【实验步骤】
(1)按上图连接好装置后,检查装置的气密性;
(2)在B装置中加入牙膏样品8.00g;
(3)先断开装置B和C,打开K1,关闭K2,通入空气一段时间,目的是赶尽装置中的空气,再接上装置B和C;关闭K1,打开K2(选填“打开”或“关闭”),向牙膏样品中滴入10%的盐酸,至不再产生气泡为止,停止滴加盐酸;然后再打开K1,关闭K2(选填“打开”或“关闭”),缓缓通入空气至C中不再产生沉淀为止,目的是将反应生成的二氧化碳气体赶到装置C中充分反应.
(4)将C装置中的固液混合物过滤、洗涤、烘干后称量其质量;
(5)重复实验.
【实验数据】重复实验,3次数据记录如下:
【实验分析及数据处理】
(1)装置A的作用是CO2+2NaOH=Na2CO3+H2O(用化学方程式表示),若没有A装置,则测定结果将偏大(选填“偏大”、“偏小”或“不变”).
(2)装置B中产生气体的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)装置D的作用是防止空气中的二氧化碳气体进入装置C中,产生误差.
(4)据上表数据,取D装置中沉淀质量的平均值为3.94g,目的是减小偶然误差,使实验数据更准确;由产生沉淀的质量可计算出反应生成二氧化碳的质量为0.88g,然后可求出牙膏样品中CaCO3的质量分数为25%.
【实验探究一】某品牌牙膏中是否含有CaCO3?
【查阅资料】二氧化硅不与稀盐酸反应
【实验方案】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,滴加稀盐酸 | ①产生大量气泡 | 该牙膏样品中含有CaCO3 |
| ②把生成的气体通入澄清石灰水中 | ②石灰水变浑浊 |
【实验装置】利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.

【友情提示】
(1)氢氧化钡跟氢氧化钙的性质类似,CO2+Ba(OH)2═BaCO3↓+H2O;
(2)CO2的相对分子质量为44,CaCO3的相对分子质量为100,BaCO3的相对分子质量为197;
(3)以上药品均足量,且每步反应或作用都是完全的.
【实验步骤】
(1)按上图连接好装置后,检查装置的气密性;
(2)在B装置中加入牙膏样品8.00g;
(3)先断开装置B和C,打开K1,关闭K2,通入空气一段时间,目的是赶尽装置中的空气,再接上装置B和C;关闭K1,打开K2(选填“打开”或“关闭”),向牙膏样品中滴入10%的盐酸,至不再产生气泡为止,停止滴加盐酸;然后再打开K1,关闭K2(选填“打开”或“关闭”),缓缓通入空气至C中不再产生沉淀为止,目的是将反应生成的二氧化碳气体赶到装置C中充分反应.
(4)将C装置中的固液混合物过滤、洗涤、烘干后称量其质量;
(5)重复实验.
【实验数据】重复实验,3次数据记录如下:
| 实验次数 | 实验1 | 实验2 | 实验3 |
| D装置中沉淀质量(g) | 3.93 | 3.94 | 3.95 |
(1)装置A的作用是CO2+2NaOH=Na2CO3+H2O(用化学方程式表示),若没有A装置,则测定结果将偏大(选填“偏大”、“偏小”或“不变”).
(2)装置B中产生气体的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)装置D的作用是防止空气中的二氧化碳气体进入装置C中,产生误差.
(4)据上表数据,取D装置中沉淀质量的平均值为3.94g,目的是减小偶然误差,使实验数据更准确;由产生沉淀的质量可计算出反应生成二氧化碳的质量为0.88g,然后可求出牙膏样品中CaCO3的质量分数为25%.
14.下列说法不正确的是( )
| A. | 原子可以直接构成物质,也可以先构成分子,再由分子构成物质 | |
| B. | 汤姆森的原子模型反映了原子的真实结构 | |
| C. | 卢瑟福的α粒子散射实验现象可证明原子核体积“很小”,质量“很大” | |
| D. | 不同类原子的核内质子数一定不同 |
