题目内容
17.某化学小组进行溶液的配制的步骤,配制150g质量分数为10%的氢氧化钠溶液.(1)计算:需要氢氧化钠固体的质量为15g,水的体积为135 mL.
(2)第一组的结果小于10%,可能的原因C.
A.称量是左边放物体.B.仰视读量筒中的数字.C.俯视读量筒中的数字.
分析 (1)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得水的质量.
(2)溶质质量分数变小,则可能是溶质质量偏小或溶剂质量偏大,可以分析出可能造成这两个方面错误的原因进行分析解答.
解答 解:(1)溶质质量=溶液质量×溶质的质量分数,配制150g质量分数为10%的氢氧化钠溶液,需氯化钠的质量=150g×10%=15g;溶剂质量=溶液质量-溶质质量,则所需水的质量=150g-15g=135g(合135mL).
(2)A、称量是左边放物体,符合左物右码的原则,操作正确,不影响溶质质量分数的大小.
B、量取水时,仰视读量筒中的数字,读数比实际液体体积大,会造成实际量取的水的体积偏小,则使溶质质量分数偏大.
C、量取水时,俯视读量筒中的数字,读数比实际液体体积小,会造成实际量取的水的体积偏大,则使溶质质量分数偏小.
故答案为:(1)15;135;(2)C.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤(计算、称量、溶解)、注意事项等是正确解答本题的关键.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
20.小明吃食物过多消化不良,医生给他两片Mg(OH)2助消化药品,所发生化学反应是( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
1.菠菜中含乙二酸(H2C2O4),其味苦涩,能溶于水,水溶液呈酸性.过量食用菠菜容易造成人体缺钙.食用菠菜前一般先将菠菜用热水焯一焯,以降低草酸含量,除去菠菜的苦涩味.由此判断下列说法中,不正确的是( )
| A. | 该物质中三种元素的质量比为1:12:32 | |
| B. | 乙二酸由三种原子构成 | |
| C. | 加热可以增大乙二酸在水中的溶解度 | |
| D. | 乙二酸能与人体中的钙结合生成难溶于水的物质 |
12.下列图象能正确反应对应关系的是( )
| A. |  表示向等质量、等质量分数的两份稀硫酸中分别加入足量氧化镁、氢氧化镁固体 | |
| B. |  加热KNO3、Ca(OH)2的饱和溶液(不考虑溶剂的蒸发) | |
| C. | 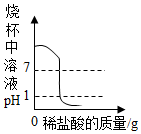 向一定质量的氢氧化钠溶液的烧杯中逐滴加入pH=1的稀盐酸至过量 | |
| D. | 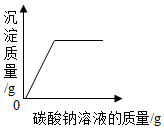 盐酸与氯化钡的混合溶液中逐滴滴入碳酸钠溶液至过量 |
6.元素观是化学的重要观念之一.下列有关元素的说法中正确的是( )
| A. | 元素是具有相同核电荷数的一类粒子的总称 | |
| B. | 元素的原子序数与该元素原子相对原子质量在数值上相同 | |
| C. | 同种元素的原子核内质子数与中子数一定相等 | |
| D. | 在物质发生化学变化时,原子的种类不变,元素也不会改变 |
7.某合金6g与足量的酸充分反应后,如果生成0.2g氢气,该合金中的元素可能是( )
| A. | Zn和Fe | B. | Cu和Au | C. | Zn和Cu | D. | Mg和A1 |