题目内容
18.溶液在生活中应用非常广泛,因而了解溶液的有关知识非常必要.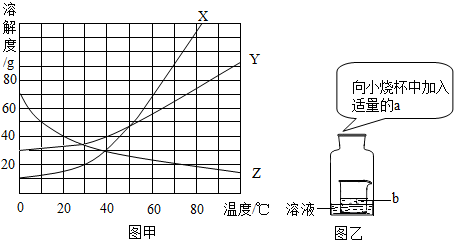
(1)小明同学欲在40℃时配制100克25%的Y物质的溶液,他能(填“能”或“不能”)到达目的.
(2)小丽用图乙所示装置进行实验.
①若广口瓶内盛有70℃X物质的不饱和溶液,b是水,a是下列B(填字母)物质,有望变成饱和溶液.
A浓硫酸 B硝酸铵 C氢氧化钠 D干冰
②若广口瓶内盛有10℃的Z物质的饱和溶液,a,b分别是镁条和稀硫酸,观察到广口瓶中溶液会出现的现象是有晶体析出(Z与其它物质不反应).
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)在40℃时,Y的溶解度是40g,其饱和溶液的溶质质量分数为:$\frac{40g}{100g+40g}×100%≈28.6%$,故能配制100克25%的Y物质的溶液,故填:能.
(2)①X的溶解度随温度的升高而增发,故广口瓶内盛有70℃X物质的不饱和溶液,b是水,要变成饱和溶液,a可以是硝酸铵,故填:B;
②Z的溶解度随温度的升高而减小,镁和稀硫酸反应放热,故广口瓶内盛有10℃的Z物质的饱和溶液,会观察到广口瓶中溶液有晶体析出,故填:有晶体析出.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.化学在环境保护、资源和能源利用等方面起着重要的作用,下列说法正确的是( )
| A. | 防止金属腐蚀是保护金属资源的唯一途径 | |
| B. | 煤、石油、天然气都属于不可再生的化石燃料 | |
| C. | 天然水经过沉降、过滤、吸附、消毒,得到的是纯水 | |
| D. | 目前计入空气污染指数的有害气体主要包括:SO2、CO2、NO2、臭氧等 |
9.物质性质决定用途.下列说法错误的是( )
| A. | 干冰升华会吸收热量,可用于人工降雨 | |
| B. | 熟石灰能和酸反应,可用于改良酸性土壤 | |
| C. | 甲醛能使蛋白质变性,可用于浸泡海鲜产品 | |
| D. | 氮气化学性质不活泼,可用于袋装食品防腐 |
6.用硬水洗涤衣物,既浪费肥皂也洗不净衣物.能降低水硬度的方法是( )
| A. | 吸附 | B. | 煮沸 | C. | 过滤 | D. | 沉淀 |
13.已知某两种物质在一定条件下发生化学反应,其微观示意图如下,下列说法正确的是( )
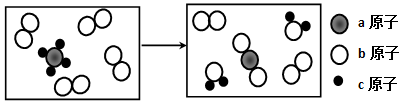

| A. | 反应前后分子的种类、个数都发生改变 | |
| B. | 该反应不是置换反应 | |
| C. | 参加反应的两种分子的个数比为4:1 | |
| D. | 该反应中生成物有单质和化合物 |
3. 化验员对某市售补钙剂进行检验,想测定其含量是否达标,如图是某补钙药品的部分说明书.在实验室中取10片钙片研碎后放于烧杯中,将100g稀盐酸分五次依次加入到烧杯中,并不断搅拌,称量,将得到的有关数据记录如下(钙片中其它成分不与稀盐酸反应)
化验员对某市售补钙剂进行检验,想测定其含量是否达标,如图是某补钙药品的部分说明书.在实验室中取10片钙片研碎后放于烧杯中,将100g稀盐酸分五次依次加入到烧杯中,并不断搅拌,称量,将得到的有关数据记录如下(钙片中其它成分不与稀盐酸反应)
请你根据题给信息和表中数据,回答下列问题:
(1)实验过程中将钙片研碎的目的是:增大接触面积,使其充分反应.
(2)完全反应后,产生二氧化碳的质量为3.52g
(3)试通过计算说明(写出具体计算过程)
①该品牌钙片含量是否达标
②所用稀盐酸溶质的质量分数
(4)如果按用量服用,服用者每天通过该补钙剂摄入钙元素的质量为0.64g.
 化验员对某市售补钙剂进行检验,想测定其含量是否达标,如图是某补钙药品的部分说明书.在实验室中取10片钙片研碎后放于烧杯中,将100g稀盐酸分五次依次加入到烧杯中,并不断搅拌,称量,将得到的有关数据记录如下(钙片中其它成分不与稀盐酸反应)
化验员对某市售补钙剂进行检验,想测定其含量是否达标,如图是某补钙药品的部分说明书.在实验室中取10片钙片研碎后放于烧杯中,将100g稀盐酸分五次依次加入到烧杯中,并不断搅拌,称量,将得到的有关数据记录如下(钙片中其它成分不与稀盐酸反应)| 稀盐酸的质量/g | 0 | 20 | 40 | 60 | 80 | 100 |
| 烧杯中剩余物质质量/g | 10 | 29.12 | 48.24 | 67.36 | 86.48 | 106.48 |
(1)实验过程中将钙片研碎的目的是:增大接触面积,使其充分反应.
(2)完全反应后,产生二氧化碳的质量为3.52g
(3)试通过计算说明(写出具体计算过程)
①该品牌钙片含量是否达标
②所用稀盐酸溶质的质量分数
(4)如果按用量服用,服用者每天通过该补钙剂摄入钙元素的质量为0.64g.
7.下列物质的主要成分与化学式相符合的是( )
| A. | 纯碱NaOH | B. | 天然气CO | C. | 石灰石Ca(OH)2 | D. | 小苏打NaHCO3 |
8.银针曾是中医针灸的常用器械,银的元素符号是( )
| A. | Ag | B. | Hg | C. | Au | D. | Sn |