题目内容
7.生活中处处有化学,请你用所学的化学知识来解释:(1)新装修的房屋内空气中通常含有较多的甲醛(CH2O)、苯(C6H6)等有毒物质.这两种物质都属于有机物(填“无机物”或“有机物”);
(2)在自行车表面喷一层油漆可防锈,其原理是隔绝空气和水;
(3)生石灰能与水反应,常用作食品干燥剂,该反应的化学方程式是:CaO+H2O=Ca(OH)2;
(4)使用天然气(主要成分是甲烷)做燃料时发生反应的化学方程式是:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(5)CO在工业上用于冶炼金属,写出一氧化碳在高温下还原赤铁矿(主要成分氧化铁)的化学方程式是:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
分析 (1)根据有机物的定义进行判断,
(2)根据钢铁生锈的条件进行分析,
(3)根据反应的原理、反应物、生成物进行书写,
(4)根据反应物、生成物以及反应的条件书写化学方程式,
(5)根据一氧化碳在高温下还原赤铁矿(主要成分氧化铁)生成铁和二氧化碳解答.
解答 解:(1)有机物中都含有碳元素,一氧化碳、二氧化碳、碳酸钙等除外,故答案为:有机物,
(2)钢铁在潮湿的空气中容易生锈,刷漆是为了隔绝空气和水,故答案为:隔绝空气和水,
(3)生石灰和水发生化合反应生成氢氧化钙,故答案为:CaO+H2O=Ca(OH)2,
(4)天然气和氧气在点燃的条件下生成二氧化碳和水,故答案为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(5)一氧化碳在高温下还原赤铁矿(主要成分氧化铁)生成铁和二氧化碳,化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
故答案为:(1)有机物;(2)隔绝空气和水;(3)CaO+H2O=Ca(OH)2;(4)CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;(5)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
点评 本题主要考查了对有机物的判断以及金属的锈蚀和防护等方面的知识,要加以识记.

练习册系列答案
相关题目
18.下列关于水的变化中,与其他变化有根本区别的一种是( )
| A. | 蒸发水 | B. | 电解水 | C. | 冰雪融化 | D. | 水结成冰 |
2.我国科学家屠呦呦从中药中分离出青蒿素应用于疟疾治疗,获得2015年诺贝尔生理学或医学奖.下列有关青蒿素(C15H22O5)的说法正确的是( )
| A. | 青蒿素是氧化物 | |
| B. | 每个青蒿素分子由42个原子构成 | |
| C. | 青蒿素中碳、氢、氧三种元素的质量比是15:22:5 | |
| D. | 青蒿素的相对分子质量为282g |
12.二氧化碳与二氧化硫同为非金属氧化物,某兴趣小组用类比法进行如下探究:
探究一 SO2的制取
(1)实验室常用固体亚硫酸钠(Na2SO3)与稀硫酸在常温下反应制取二氧化硫,选择发生装置主要应该考虑的因素是A、B(填序号,可多选).
A.反应物的状态 B.反应条件 C.气体密度 D.气体溶解性
(2)探究二氧化硫性质,该兴趣小组进行了如图1所示的实验.
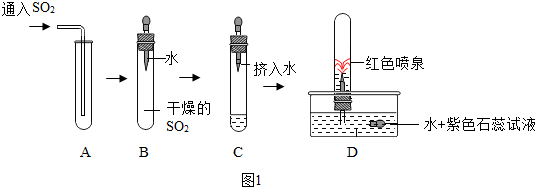
通过上述实验,可推测SO2气体的性质有:
①SO2密度比空气大.
②SO2能溶于水等合理答案.
探究二 CO2和SO2性质的比较
兴趣小组设计并进行如图2实验,探究比较CO2和SO2的化学性质.
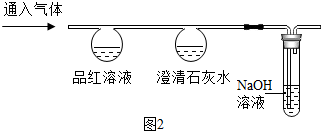
(3)由实验可知:
①二氧化硫能与澄清石灰水反应,生成亚硫酸钙(CaSO3)和水,写出该反应的化学方程式SO2+Ca(OH)2=CaSO3↓+H2O.
②鉴别CO2和SO2的方法是将气体分别通入品红溶液,红色褪去是SO2,无明显变化的是CO2③实验Ⅱ中NaOH溶液的作用是吸收尾气,防止其吸收尾气,防止其污染空气.
探究三 测定空气中SO2的含量,探究小组进行如下实验
【查阅资料】①碘水遇淀粉变蓝色.
②二氧化硫与碘水反应的化学方程式为:SO2+I2+2H2O=H2SO4+2HI
(SO2、I2的相对分子质量分别为:64、254).
③我国环境空气质量标准中对每次空气质量测定中SO2最高浓度限值
(4)测定步骤:
Ⅰ.检查装置的气密性.
Ⅱ.向试管中加入1g溶质质量分数为0.0127%的碘水,用适量的蒸馏水稀释,再滴入2-3滴淀粉溶液,配制成稀溶液.
Ⅲ.在指定地点用注射器抽取空气140次注入上述试管中(假设每次抽气500mL)
由实验可知:
①当溶液由蓝色变成无色时反应恰好完全.
②由此可计算空气中SO2的含量0.46mg/m3(结果精确至0.01),所测地点的空气中SO2的含量属于二级标准(填上表中所列举的等级).
探究一 SO2的制取
(1)实验室常用固体亚硫酸钠(Na2SO3)与稀硫酸在常温下反应制取二氧化硫,选择发生装置主要应该考虑的因素是A、B(填序号,可多选).
A.反应物的状态 B.反应条件 C.气体密度 D.气体溶解性
(2)探究二氧化硫性质,该兴趣小组进行了如图1所示的实验.

通过上述实验,可推测SO2气体的性质有:
①SO2密度比空气大.
②SO2能溶于水等合理答案.
探究二 CO2和SO2性质的比较
兴趣小组设计并进行如图2实验,探究比较CO2和SO2的化学性质.

| 实验Ⅰ | 实验Ⅱ | |
| 通入CO2 | 通入SO2 | |
| 品红溶液 | 无明显变化 | 红色褪为无色 |
| 澄清石灰水 | 白色浑浊 | 白色浑浊 |
①二氧化硫能与澄清石灰水反应,生成亚硫酸钙(CaSO3)和水,写出该反应的化学方程式SO2+Ca(OH)2=CaSO3↓+H2O.
②鉴别CO2和SO2的方法是将气体分别通入品红溶液,红色褪去是SO2,无明显变化的是CO2③实验Ⅱ中NaOH溶液的作用是吸收尾气,防止其吸收尾气,防止其污染空气.
探究三 测定空气中SO2的含量,探究小组进行如下实验
【查阅资料】①碘水遇淀粉变蓝色.
②二氧化硫与碘水反应的化学方程式为:SO2+I2+2H2O=H2SO4+2HI
(SO2、I2的相对分子质量分别为:64、254).
③我国环境空气质量标准中对每次空气质量测定中SO2最高浓度限值
| SO2最高浓度限值(单位mg/m3) | ||
| 一级标准 | 二级标准 | 三级标准 |
| 0.15 | 0.50 | 0.70 |
Ⅰ.检查装置的气密性.
Ⅱ.向试管中加入1g溶质质量分数为0.0127%的碘水,用适量的蒸馏水稀释,再滴入2-3滴淀粉溶液,配制成稀溶液.
Ⅲ.在指定地点用注射器抽取空气140次注入上述试管中(假设每次抽气500mL)
由实验可知:
①当溶液由蓝色变成无色时反应恰好完全.
②由此可计算空气中SO2的含量0.46mg/m3(结果精确至0.01),所测地点的空气中SO2的含量属于二级标准(填上表中所列举的等级).
16.遂川狗牯脑茶,是我省珍贵名茶之一.新鲜狗牯脑茶用沸水冲泡后会散发清香,说明( )
| A. | 分子可以再分 | B. | 分子的质量很小 | C. | 分子不停运动 | D. | 分子间有间隙 |
 向盛有100g稀硫酸的烧杯中加入一定量的镁粉,固体完全溶解后,固体完全溶解后,再向所得溶液中加入NaOH溶液,所得沉淀质量与加入NaOH溶液的质量关系如图所示
向盛有100g稀硫酸的烧杯中加入一定量的镁粉,固体完全溶解后,固体完全溶解后,再向所得溶液中加入NaOH溶液,所得沉淀质量与加入NaOH溶液的质量关系如图所示