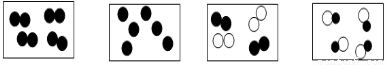
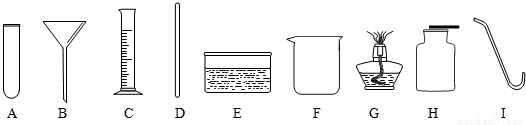
题目内容
利用如下图装置进行“硫燃烧”的实验: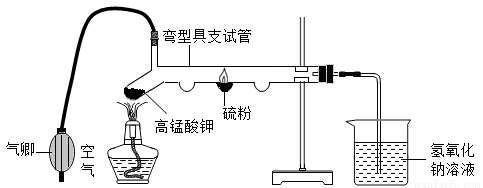
(1)用气卿不断地向弯型具支试管中鼓入空气,同时用酒精灯给硫粉加热至燃烧,可观察到_______;然后停止鼓入空气,再用酒精灯给高锰酸钾加热,使硫在纯氧中继续燃烧,观察到_______.实验结束后,先______,再熄灭酒精灯,目的是__________
(2)用烧杯中的氢氧化钠溶液的作用 ___________________(氢氧化钠与二氧化硫反应生成亚硫酸钠和水)。
(3)该实验装置的主要优点是 __________________
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出化学反应的文字表达式:________________________________________________。
小芳发现,氯酸钾与氧化铜混合加热,也能较快地产生氧气,于是进行如下探究:
【提出猜想】除MnO2、CuO外,Fe2O3也可以作KClO3分解的催化剂。
【完成实验】按下表进行实验:测定分解温度(分解温度越低,催化效果越好)。
实验编号 | 实验药品 | 分解温度(℃) |
① | KClO3 | 580 |
② | KClO3、MnO2(质量比1:1) | 350 |
③ | KClO3、CuO (质量比l:1) | 370 |
④ | KClO3、Fe2O3(质量比1:1) | 390 |
【分析数据、得出结论】
(1)由实验_________________与实验④对比,证明猜想合理。
(2)实验所用的三种金属氧化物,催化效果最好的是___________________。
【反思】
(1)若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后质量和____________不改变。
(2)同种催化剂,颗粒大小可能影响催化效果,请你设计实验方案进行验证:
________________________________________________________________________;
(3)同种催化剂,还有哪些因素可能影响催化效果,请你再探究 (探究一种因素即可)。
①你的假设:_______________________________________;
②你的实验方案:______________________________________________________________。