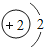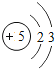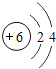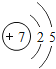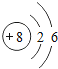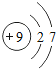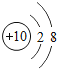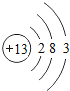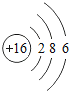题目内容
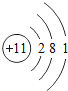
核电荷数为1﹣18的原子结构示意图等信息如下,请回答下列问题:
第一周期 | 1H
| 2He
| |||||||
第二周期 | 3Li
| 4Be
| 5B
| 6C
| 7N
| 8O
| 9F
| 10Ne
| |
第三周期 | 11Na
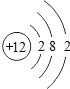
| 12Mg
| 13Al
| 14Si
| 15P
| 16S
| 17Cl
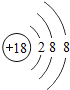
| 18Ar
| |
(1)不同种元素最本质的区别是_____(选填序号)
A质子数不同 B最外层电子数不同 C中子数不同 D相对原子质量不同
(2)在第三周期中,各原子结构的共同之处是_____;该周期中,各原子核外电子排布的变化规律是_____.
(3)在第三周期中,元素类型的变化情况是:从左到右由_____元素过渡到_____元素,并以稀有气体元素结尾.
(4)写出核外电子排布与氖原子相同的阳离子和阴离子各一个:阳离子_____,阴离子_____.
某化学兴趣小组的同学在探究金属的有关性质时,进行了如图所示实验:在A实验结束后将两支试管内的物质倒入一洁净烧杯中,一段时间后过滤。为确定过滤后得到的滤渣和滤液的成分,同学们进行了如下实验。
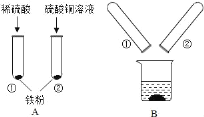
实验一:滤渣的成分是什么?
(1)甲同学取少量滤渣于试管中,加入稀硫酸,无气泡产生,证明滤渣里不含_____。乙同学通过物理方法也得到了同样的结论,请简述方法和现象_____。
实验二:滤液里的溶质有哪些?
(2)同学们认为一定有硫酸亚铁,为确定可能含有的其他溶质,同学们进行了如下实验:
实验步骤 | 实验现象 | 实验结论 |
取少量滤液,向其中加入少量铁粉 | _____ | 滤液里的溶质还有硫酸和硫酸铜 |
请写出铁与硫酸铜反应的化学方程式:_____。
(3)有同学提出可以直接观察滤液的颜色判断滤液中是否含有硫酸铜,同学们对硫酸铜溶液为什么呈蓝色很感兴趣,决定探究硫酸铜溶液中哪种粒子使溶液呈蓝色。设计的实验方案如下:
实验操作 | 实验现象 | 实验结论 |
①取少量_____溶液,观察颜色 | 溶液呈无色 | 硫酸根离子不能使溶液呈蓝色 |
②取少量硫酸铜溶液,观察颜色 | 溶液呈蓝色 | 铜离子使溶液呈蓝色 |
(4)除了(3)中实验方案外,你还能设计其他方案探究硫酸铜溶液中到底是哪种粒子使溶液呈蓝色吗?实验所需的药品和仪器任选,请简述实验操作和实验现象。
实验搡作 | 实验现象 |
_____ | _____ |