题目内容
4.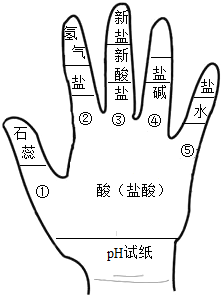 构建模型和构建知识网络是化学学习中重要的学习方法,李华同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:
构建模型和构建知识网络是化学学习中重要的学习方法,李华同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:(1)如用湿润的pH试纸测定盐酸的pH,则结果会偏大(填“偏大”、“偏小”、“无影响”).
(2)图中①的现象是:石蕊变红.
(3)写出一个符合图中③的化学方程式HCl+AgNO3=AgCl↓+HNO3.
(4)图中性质④属于复分解反应(填基本反应类型).
(5)图中⑤的性质在工业上可用于盐酸除铁锈(填用途).
分析 (1)测定盐酸的pH时,用蒸馏水湿润pH试纸后,相当于盐酸溶液被稀释,酸性减弱.
(2)酸跟石蕊指示剂反应,使其颜色变为红色.
(3)跟某些盐反应生成另外的酸和盐,前提是有一种生成物为气体或沉淀.
(4)酸与碱的反应,符合两种化合物相互交换成分生成另两种化合物的反应,是复分解反应.
(5)图中⑤的性质内容较广,可以是指盐酸与碱反应,也可以是指盐酸与金属氧化物反应.
解答 解:(1)测定盐酸的pH时,用蒸馏水湿润pH试纸后,相当于盐酸溶液被稀释,酸性减弱,则结果会偏大.
(2)酸跟石蕊指示剂反应,使其颜色变为红色.
(3)跟某些盐反应生成另外的酸和盐,前提是有一种生成物为气体或沉淀,如盐酸和硝酸银溶液反应生成氯化银和硝酸,反应的化学方程式为:HCl+AgNO3=AgCl↓+HNO3.
(4)酸与碱的反应,符合两种化合物相互交换成分生成另两种化合物的反应,是复分解反应.
(5)铁锈属于金属氧化物,与盐酸反应生成盐和水,由此性质盐酸在工业上可用于除锈.
故答案为:
(1)偏大;
(2)石蕊变红;
(3)HCl+AgNO3=AgCl↓+HNO3;
(4)复分解;
(5)盐酸除铁锈.
点评 盐酸是酸的代表物质,要熟记酸的通性,要求同学们能写出每一项性质的化学方程式.

练习册系列答案
相关题目
14.对下列实验事实的解释正确的是( )
| 选项 | 事实 | 解释 |
| A | 铜导线夏天会变长 | 温度升高,分子间间隔变大 |
| B | 一氧化碳和二氧化碳的化学性质不同 | 不同种分子,化学性质不同 |
| C | 某化肥加熟石灰研磨,没有嗅到氨味 | 无氨气放出,一定不是氮肥 |
| D | 长期盛放NaOH溶液的试剂瓶口,出现白色粉末 | 氢氧化钠发生了潮解 |
| A. | A | B. | B | C. | C | D. | D |
9.下列化学用语表示正确的是( )
| A. | 2个氮分子:2N | B. | 2个氮原子:N2 | ||
| C. | 氧化镁中镁元素化合价为+2:$\stackrel{+2}{Mg}$O | D. | 2个氢氧根离子:2OH |
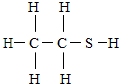 乙硫醇是2000年版吉尼斯世界纪录中收录的最臭的物质.空气中仅含五百亿分之一的乙硫醇时,其臭味就可嗅到,通常被加入液化煤气中做臭味指示剂.乙硫醇的结构式见图,请回答下列问题:
乙硫醇是2000年版吉尼斯世界纪录中收录的最臭的物质.空气中仅含五百亿分之一的乙硫醇时,其臭味就可嗅到,通常被加入液化煤气中做臭味指示剂.乙硫醇的结构式见图,请回答下列问题:
 人类的日常生活和工农业生产离不开水和溶液.请回答:
人类的日常生活和工农业生产离不开水和溶液.请回答: