题目内容
19.实验室常用如图所示装置来制取气体,请回答下列问题.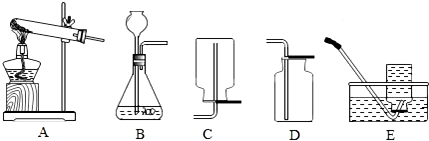
(1)写出用 A 装置制取氧气的化学方程式.
(2)B装置中长颈漏斗必须伸入到液面以下的原因是什么?
(3)从上述装置中选出实验室制取二氧化碳的一组装置为BD.写出该反应的化学方程式.
分析 (1)根据装置A的特点来分析;
(2)根据B装置中长颈漏斗必须伸入液面以下的原因是防止气体从长颈漏斗逸出进行分析;
(3)根据制取二氧化碳的反应原理、二氧化碳的性质来分析.
解答 解:(1)A装置使用固体加热制取氧气,试管口没有棉花团,所以是加热氯酸钾与二氧化锰的混合物制取氧气,反应原理为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;故填:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(2)B装置中长颈漏斗必须伸入液面以下的原因是防止气体从长颈漏斗逸出;故填:防止气体从长颈漏斗逸出;
(3)实验室中常用大理石或石灰石与稀盐酸反应制取二氧化碳,属于固液常温下制取气体,故选择装置B;二氧化碳的密度比空气大,能溶于水,所以用向上排空气法来收集;碳酸钙与盐酸反应生成氯化钙、水和二氧化碳;故填:BD;CaCO3+2HCl═CaCl2+H2O+CO2↑.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.物质的下列性质中,需要通过化学变化才能体现的是( )
| A. | 氧化性 | B. | 延展性 | C. | 挥发性 | D. | 导热性 |
14.取6.4gMg和MgO的混合物,与一定量稀硫酸恰好完全反应,所得溶液中溶质的质量为24g,则原混合物中氧元素的质量为( )
| A. | 1.6 g | B. | 2.56 g | C. | 3.2 g | D. | 4.8 g |
11.如图图示实验基本操作错误的是( )
| A. |  倾倒液体 | B. |  读取液体体积 | C. |  检查气密性 | D. |  稀释浓硫酸 |
9.如表中,有关量的变化图象与其对应叙述相符的是( )
| A. |  向接近饱和的NaCl溶液中加入固体NaCl | |
| B. |  向等质量、等质量分数的两份稀盐酸中分别加入足量的ZnO和Zn(OH)2 | |
| C. | 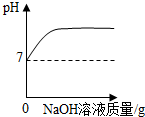 向Na2CO3溶液中加入一定溶质质量分数的NaOH溶液 | |
| D. | 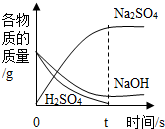 等质量、等质量分数的H2SO4溶液与NaOH溶液混合 |