题目内容
纯水清澈透明、不含杂质,而硬水含较多可溶性钙和镁的化合物.现有两瓶无色液体,分别为纯水和硬水,请你参与小雯同学对水的探究,并回答有关问题.
(1)区别纯水和硬水的方法有多种.小雯采用的方法是:分别取样于蒸发皿中,加热蒸干,有固体析出的是硬水.请你设计另一种方法(简述实验步骤、现象和结论):
(2)小雯在做实验时,发现硬水在蒸发的过程中,产生了少量气体并得到一种难溶性的固体.
【提出猜想】产生的气体可能是二氧化碳;难溶性的固体可能是碳酸盐.
【设计实验】①将生成的气体通入 中,观察到 的现象,证明产生的气体是二氧化碳.写出有关反应的化学方程式: .
②向这种难溶性的固体中滴入 ,观察到有大量的气泡产生,则这种固体可能是碳酸盐.若这种固体是碳酸钙,写出该反应的化学方程式: .
【反馈与运用】通过上述实验得到启发,在家里可用 除去热水瓶胆.
(1)区别纯水和硬水的方法有多种.小雯采用的方法是:分别取样于蒸发皿中,加热蒸干,有固体析出的是硬水.请你设计另一种方法(简述实验步骤、现象和结论):
| 实验步骤 | 实验现象 | 实验结论 |
【提出猜想】产生的气体可能是二氧化碳;难溶性的固体可能是碳酸盐.
【设计实验】①将生成的气体通入
②向这种难溶性的固体中滴入
【反馈与运用】通过上述实验得到启发,在家里可用
考点:硬水与软水,常见气体的检验与除杂方法,证明碳酸盐,书写化学方程式、文字表达式、电离方程式
专题:空气与水
分析:(1)从可用肥皂水区分硬水和软水去解答:
(2)【设计实验】
①从题目中可知:“证明产生的气体是二氧化碳.”去解答;
②从题目中:“固体可能是碳酸盐去解答;
【反馈与运用】根据(2)【设计实验】②可知水垢可以和酸反应,生成溶于水的物质去解答.
(2)【设计实验】
①从题目中可知:“证明产生的气体是二氧化碳.”去解答;
②从题目中:“固体可能是碳酸盐去解答;
【反馈与运用】根据(2)【设计实验】②可知水垢可以和酸反应,生成溶于水的物质去解答.
解答:解:(1)硬水中含有较多的钙镁化合物,易生水垢,与肥皂不易起泡沫,易起渣,而软水则与肥皂易起泡沫,所以可用肥皂水区分硬水和软水;故答案为:
(2)【设计实验】
①由题目中可知:“证明产生的气体是二氧化碳.”可知前面是二氧化碳的检验方法;通常用石灰水来检验二氧化碳,二氧化碳和石灰水反应生成不溶于水的碳酸钙和水,其化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;故答案为:澄清的石灰水 澄清石灰水变浑浊 CO2+Ca(OH)2=CaCO3+H2O;
②由题目中:“固体可能是碳酸盐”,检验碳酸盐的方法是加稀盐酸,产生二氧化碳气体,碳酸钙和稀盐酸反应生成氯化钙和水和二氧化碳,其化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑; 故答案为:稀盐酸 CaCO3+2HCl=CaCl2+CO2↑+H2O;
【反馈与运用】由(2)【设计实验】②可知水垢可以和酸反应,生成溶于水的物质,可用食醋代替稀盐酸;故答案为:食醋.
| 实验步骤 | 实验现象 | 实验结论 |
| 分别取少量于烧杯中, 加入肥皂水,搅拌 | 其中一个烧杯中产生较多的泡沫, 另一个烧杯中产生的泡沫较少 | 泡沫多的是纯水, 泡沫少的是硬水 |
①由题目中可知:“证明产生的气体是二氧化碳.”可知前面是二氧化碳的检验方法;通常用石灰水来检验二氧化碳,二氧化碳和石灰水反应生成不溶于水的碳酸钙和水,其化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;故答案为:澄清的石灰水 澄清石灰水变浑浊 CO2+Ca(OH)2=CaCO3+H2O;
②由题目中:“固体可能是碳酸盐”,检验碳酸盐的方法是加稀盐酸,产生二氧化碳气体,碳酸钙和稀盐酸反应生成氯化钙和水和二氧化碳,其化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑; 故答案为:稀盐酸 CaCO3+2HCl=CaCl2+CO2↑+H2O;
【反馈与运用】由(2)【设计实验】②可知水垢可以和酸反应,生成溶于水的物质,可用食醋代替稀盐酸;故答案为:食醋.
点评:本题难度不大,掌握硬水的成分、硬水与软水的区别、及转化方法是正确解答此类题的关键.

练习册系列答案
相关题目
下列反应属于置换反应的是( )
| A、Si+2NaOH+H2O=Na2SiO3+2H2↑ | ||||
B、CO+CuO
| ||||
C、C+H2O
| ||||
D、CH4+Cl2
|
化学用语是学习化学的主要工具,是国际通用的化学语言.下列化常用语中,正确的是( )
| A、两个氧分子:O2 |
| B、氢氧化铁的化学式:Fe(OH)3 |
| C、CO2中氧元素的化合价为+2价 |
| D、水通电得到氧气的化学方程式是2H2O=O2↑+2H2↑ |
下列哪种物质会对空气造成污染( )
| A、铜绿受热分解时生成的气体 |
| B、植物光合作用放出的气体 |
| C、工业制氧气时排放的气体 |
| D、燃放烟花时产生的刺激性气味的气体 |
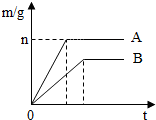 取质量相等的镁、铁两种金属,分别投入两个各装有50mL盐酸的烧杯,反应产生氢气的质量(m)与反应时间(t)的关系如图所示,反应结束后无固体剩余.
取质量相等的镁、铁两种金属,分别投入两个各装有50mL盐酸的烧杯,反应产生氢气的质量(m)与反应时间(t)的关系如图所示,反应结束后无固体剩余. 有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如表部分数据和图象.
有一种石灰石样品的成分是CaCO3和SiO2.课外小组同学将100g盐酸分5次加入到35g石灰石样品中(已知SiO2不与盐酸反应),得到如表部分数据和图象.