题目内容
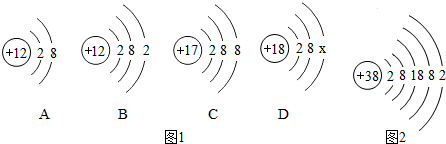
19.物质的结构决定性质,下列说法正确的是( )| A. | 石墨转化为金刚石是由于原子种类改变 | |
| B. | Na和Na+属于同种元素是由于电子数相同 | |
| C. | CO2和CO的化学性质不同是由于分子间隔不同 | |
| D. | FeCl3、Fe2(SO4)3溶液都能与NaOH溶液发生类似反应,是因为所含阳离子相同 |
分析 A、根据金刚石和石墨的构成解答;
B、根据钠原子和钠离子的属于同种元素的因素解答;
C、根据一氧化碳和二氧化碳的性质差异解答;
D、根据物质的组成解答.
解答 解:A、石墨转化为金刚石是由于原子排列方式发生改变,不是原子改变,错误;
B、Na和Na+属于同种元素是由于核内质子数相同,错误;
C、CO2和CO的化学性质不同是由于分子构成不同,错误;
D、FeCl3、Fe2(SO4)3溶液都能与NaOH溶液发生类似反应,是因为所含阳离子相同,正确;
故选D.
点评 掌握物质的微观构成是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.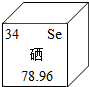 元素周期表中硒元素的某些信息如图所示,下列有关硒的说法不正确的是( )
元素周期表中硒元素的某些信息如图所示,下列有关硒的说法不正确的是( )
 元素周期表中硒元素的某些信息如图所示,下列有关硒的说法不正确的是( )
元素周期表中硒元素的某些信息如图所示,下列有关硒的说法不正确的是( )| A. | 是金属元素 | B. | 原子核内有34个质子 | ||
| C. | 相对原子质量为78.96 | D. | 硒是人体必须的微量元素 |
14.叠氮化钠(NaN3)被广泛应用于汽车安全气囊,某化学小组同学对其进行下列研究.
【查阅资料】:
①NaN3受撞击会迅速分解生成Na、N2,写出该反应的化学方程式2NaN3$\frac{\underline{\;撞击\;}}{\;}$2Na+3N2↑.
②NaN3遇盐酸、H2SO4溶液无气体生成;
③碱石灰是CaO和 NaOH的混合物;
④NaN3工业上制备方法是:将金属钠与液态氨反应制得NaNH2,再将NaNH2与N2O反应可生成NaN3、NaOH和气体X,该反应的化学方程式为2NaNH2+N2O=NaN3+NaOH+X;则X的化学式为NH3.
【问题探究】:(一)测定某工业级NaN3样品中Na2CO3的质量分数
(1)工业级NaN3中常含有少量的Na2CO3,其原因是(用化学方程式表示)2NaOH+CO2═Na2CO3+H2O;
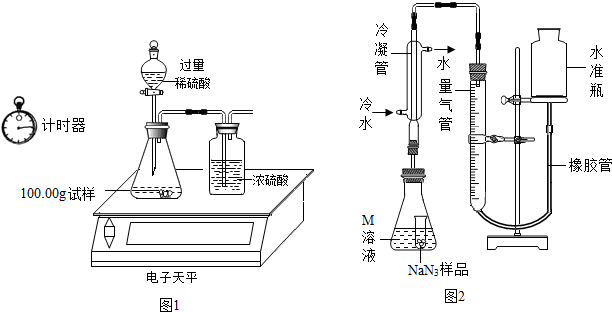
(2)某同学设计如图1装置测出碳酸钠的质量分数,其实验数据记录如表:
①写出锥形瓶中发生的反应方程式:Na2CO3+H2SO4=Na2SO4+H2O+CO2↑;
②若无浓硫酸的洗气装置,会使测定的结果偏大(填“偏大”、“偏小”或“不变”);
③利用表中数据计算出碳酸钠的质量分数为5.3%.
【问题探究】:(二)测定某工业级样品中NaN3的质量分数
小谈同学精确称量0.140g NaN3样品,设计如图2装置测定其质量分数.
已知2NaN3→3N2(NaN3中的N全部转化为N2,其他产物略),反应中放出大量的热.
(1)检查该装置气密性的方法是:连接好装置,从水准管注水,左右两边出现稳定的液面差,说明气密性良好.
(2)使用冷水冷凝的目的是:使水蒸气液化(或除去水蒸气);.
(3)倾斜锥形瓶使小试管中的NaN3样品与M溶液接触充分反应. 常温下测得量气管读数为67.2mL(N2的密度为1.25g/L),则实验中选用的量气管规格合适的是A(填字母序号).
A.100mL B.1L C.2L
(4)计算工业级样品中NaN3的质量分数(写出计算过程,结果保留0.1%).
【查阅资料】:
①NaN3受撞击会迅速分解生成Na、N2,写出该反应的化学方程式2NaN3$\frac{\underline{\;撞击\;}}{\;}$2Na+3N2↑.
②NaN3遇盐酸、H2SO4溶液无气体生成;
③碱石灰是CaO和 NaOH的混合物;
④NaN3工业上制备方法是:将金属钠与液态氨反应制得NaNH2,再将NaNH2与N2O反应可生成NaN3、NaOH和气体X,该反应的化学方程式为2NaNH2+N2O=NaN3+NaOH+X;则X的化学式为NH3.
【问题探究】:(一)测定某工业级NaN3样品中Na2CO3的质量分数
(1)工业级NaN3中常含有少量的Na2CO3,其原因是(用化学方程式表示)2NaOH+CO2═Na2CO3+H2O;
(2)某同学设计如图1装置测出碳酸钠的质量分数,其实验数据记录如表:
| 称量项目 | 称量时间 | 质量(g) |
| 试样 | 100.00 | |
| 装置+稀硫酸质量 | 241.20 | |
| 装置+稀硫酸质量+试样 | 反应开始后15秒 | 339.20 |
| 装置+稀硫酸质量+试样 | 反应开始后35秒 | 339.00 |
| 装置+稀硫酸质量+试样 | 反应开始后55秒 | 339.00 |
②若无浓硫酸的洗气装置,会使测定的结果偏大(填“偏大”、“偏小”或“不变”);
③利用表中数据计算出碳酸钠的质量分数为5.3%.
【问题探究】:(二)测定某工业级样品中NaN3的质量分数
小谈同学精确称量0.140g NaN3样品,设计如图2装置测定其质量分数.
已知2NaN3→3N2(NaN3中的N全部转化为N2,其他产物略),反应中放出大量的热.
(1)检查该装置气密性的方法是:连接好装置,从水准管注水,左右两边出现稳定的液面差,说明气密性良好.
(2)使用冷水冷凝的目的是:使水蒸气液化(或除去水蒸气);.
(3)倾斜锥形瓶使小试管中的NaN3样品与M溶液接触充分反应. 常温下测得量气管读数为67.2mL(N2的密度为1.25g/L),则实验中选用的量气管规格合适的是A(填字母序号).
A.100mL B.1L C.2L
(4)计算工业级样品中NaN3的质量分数(写出计算过程,结果保留0.1%).

4. 化学兴趣小组的同学对如图的某膨化食品包装袋内气体的成分进行探究,请你参与他们的探究,并回答下列问题.
化学兴趣小组的同学对如图的某膨化食品包装袋内气体的成分进行探究,请你参与他们的探究,并回答下列问题.
【提出问题】包装袋内的气体成分是什么?
【查阅资料】1在膨化食品包装袋内填充气体的目的可能是保护气,延长食品保质期.
2镁能在氮气中燃烧,反应生成氮化镁(Mg3N2)固体,氮化镁在常温下能与水反应生成氨气和一种难溶性碱,氨气极易溶于水,形成氨水.
【猜想与假设】包装袋内的气体为:猜想1:空气;猜想2:CO2;猜想3:N2
【实验设计】
实验一:甲用注射器收集了一瓶气体,将燃着的小木条伸入集气瓶中,若现象为燃着的小木条熄灭,则猜想1不成立.乙认为甲的实验还不能确定包装袋内的气体到底是什么成分,理由是CO2和N2都能使燃着的小木条熄.为此乙用同样的方法收集了两瓶气体,设计了以下方案进行实验.
实验二:
【交流讨论】试写出氮化镁与水反应的化学方程式3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.你认为包装袋内的气体应该具有的性质是化学性质稳定、无毒.
 化学兴趣小组的同学对如图的某膨化食品包装袋内气体的成分进行探究,请你参与他们的探究,并回答下列问题.
化学兴趣小组的同学对如图的某膨化食品包装袋内气体的成分进行探究,请你参与他们的探究,并回答下列问题.【提出问题】包装袋内的气体成分是什么?
【查阅资料】1在膨化食品包装袋内填充气体的目的可能是保护气,延长食品保质期.
2镁能在氮气中燃烧,反应生成氮化镁(Mg3N2)固体,氮化镁在常温下能与水反应生成氨气和一种难溶性碱,氨气极易溶于水,形成氨水.
【猜想与假设】包装袋内的气体为:猜想1:空气;猜想2:CO2;猜想3:N2
【实验设计】
实验一:甲用注射器收集了一瓶气体,将燃着的小木条伸入集气瓶中,若现象为燃着的小木条熄灭,则猜想1不成立.乙认为甲的实验还不能确定包装袋内的气体到底是什么成分,理由是CO2和N2都能使燃着的小木条熄.为此乙用同样的方法收集了两瓶气体,设计了以下方案进行实验.
实验二:
| 实验步骤 | 实验现象 | 实验结论 |
| 向其中一瓶气体中滴加澄清石灰水,振荡,观察现象. | 澄清石灰水变浑浊 | 猜想2不成立 |
| ①将点燃的镁条伸入另一瓶气体中燃烧. ②完全反应后取少量固体物质加入足量的蒸馏水溶解,并滴入无色酚酞溶液,振荡观察现象. | ①镁条剧烈燃烧,发出耀眼的白光. ②溶液就变红,同时有白色沉淀产生 | 猜想3成立 |
8.除去下列物质中的杂质,所选用的试剂和操作方法都正确的是( )
| 选项 | 物质 | 杂质(少量) | 试剂及操作方法 |
| A | 氧化钙 | 石灰石 | 加入稀盐酸 |
| B | 氨气 | 水蒸气 | 通过足量的氢氧化钠固体 |
| C | 稀盐酸 | 稀硝酸 | 加入过量的硝酸银溶液,过滤 |
| D | CO2 | CO | 通入足量氧气、点燃 |
| A. | A | B. | B | C. | C | D. | D |