题目内容
物质的用途和使用方法等与其性质密切相关.
(1)铁在生活中可用于制作炊具,因为它有良好的延展性和 性.
(2)氢氧化钙常用做建筑材料,因为其吸收二氧化碳会生成坚固的 (写化学式).
(3)复方氢氧化铝可用于治疗胃酸过多症,用化学方程式表示其原因: .
(4)“漂白粉”可以快速漂除衣物污渍,其有效成分为次氯酸钠(NaClO).若与“洁厕灵”混用,易产生一种有毒气体,化学方程式为NaClO+2HCl═NaCl+X↑+H2O,则X的化学式为 .
(1)铁在生活中可用于制作炊具,因为它有良好的延展性和
(2)氢氧化钙常用做建筑材料,因为其吸收二氧化碳会生成坚固的
(3)复方氢氧化铝可用于治疗胃酸过多症,用化学方程式表示其原因:
(4)“漂白粉”可以快速漂除衣物污渍,其有效成分为次氯酸钠(NaClO).若与“洁厕灵”混用,易产生一种有毒气体,化学方程式为NaClO+2HCl═NaCl+X↑+H2O,则X的化学式为
考点:金属的物理性质及用途,碱的化学性质,质量守恒定律及其应用,书写化学方程式、文字表达式、电离方程式
专题:物质的性质与用途
分析:(1)运用铁在生活中可用于制作炊具,因为它有良好的延展性和导热性解答;
(2)根据氢氧化钙的性质进行解答;
(3)胃酸的成分是盐酸,根据酸碱中和写出化学方程式;
(4)根据质量守恒定律反应前后原子的种类及数目不变分析X的化学式.
(2)根据氢氧化钙的性质进行解答;
(3)胃酸的成分是盐酸,根据酸碱中和写出化学方程式;
(4)根据质量守恒定律反应前后原子的种类及数目不变分析X的化学式.
解答:解:(1)铁在生活中可用于制作炊具,因为它有良好的延展性和导热性,故答案为:导热;
(2)二氧化碳与氢氧化钙反应生成水和碳酸钙,碳酸钙的化学式为CaCO3;故答案为:CaCO3;
(3)胃酸的成分是盐酸,与氢氧化铝反应生成氯化铝和水,其反应的方程式为:Al(OH)3+3HCl═AlCl3+3H2O;故答案为:Al(OH)3+3HCl═AlCl3+3H2O;
(4)在化学方程式NaClO+2HCl═NaCl+X↑+H2O中,反应前钠原子、氯原子、氧原子、氢原子的个数分别为1个、3个、1个、2个,反应后除X外钠原子、氯原子、氧原子、氢原子的个数分别为1个、1个、1个、2个.由于反应前后原子种类和数量都不改变.所以,X中有2个氯原子,故X的化学式为Cl2.故答案为:Cl2.
(2)二氧化碳与氢氧化钙反应生成水和碳酸钙,碳酸钙的化学式为CaCO3;故答案为:CaCO3;
(3)胃酸的成分是盐酸,与氢氧化铝反应生成氯化铝和水,其反应的方程式为:Al(OH)3+3HCl═AlCl3+3H2O;故答案为:Al(OH)3+3HCl═AlCl3+3H2O;
(4)在化学方程式NaClO+2HCl═NaCl+X↑+H2O中,反应前钠原子、氯原子、氧原子、氢原子的个数分别为1个、3个、1个、2个,反应后除X外钠原子、氯原子、氧原子、氢原子的个数分别为1个、1个、1个、2个.由于反应前后原子种类和数量都不改变.所以,X中有2个氯原子,故X的化学式为Cl2.故答案为:Cl2.
点评:本题主要考查物质的性质和用途,物质具有多种性质,解答时应该理解物质的用途是由物质的哪种性质决定的;对于化学方程式的考查始终是中考的热点.

练习册系列答案
相关题目
认识燃烧原理可以合理利用和控制燃烧反应.下列说法中正确的是( )
| A、增大可燃物与空气的接触面积,可促进燃烧 |
| B、物质与氧气反应时都会发生燃烧 |
| C、只有燃烧反应能将化学能转化为热能 |
| D、煤炉生火时,用木材引燃是为了提高煤的着火点 |
下列属于物理变化的是( )
| A、浓硫酸使白纸变黑 |
| B、铜质器皿表面生绿斑 |
| C、氢氧化钠固体吸水潮解 |
| D、石灰浆粉刷墙壁后,墙壁变硬 |
人类认识化学经过了漫长的过程,下列物质的排列顺序符合这一过程的是( )
①石器 ②瓷器 ③青铜器 ④铁器 ⑤纳米材料.
①石器 ②瓷器 ③青铜器 ④铁器 ⑤纳米材料.
| A、①②③④⑤ |
| B、①②④③⑤ |
| C、②①③④⑤ |
| D、②①④③⑤ |
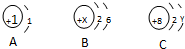 如图为A、B、C三种粒子的结构示意图:
如图为A、B、C三种粒子的结构示意图: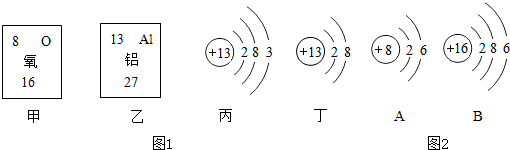
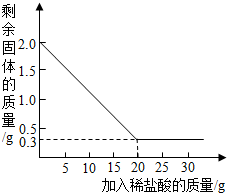 某化学兴趣小组的同学在综合实践活动中了解到,某石灰石原料,其中只含有的一种杂质是二氧化硅(二氧化硅不溶于水,不能与盐酸反应,高温下不发生分解反应).为了测定该石灰石的纯度,兴趣小组取用2g这种石灰石样品,用实验室现有的稀盐酸30g分次加入,充分反应后,经过滤、干燥等操作后称量,每次稀盐酸用量及剩余固体的质量见下表(利用实验数据绘制的图象如图所示)
某化学兴趣小组的同学在综合实践活动中了解到,某石灰石原料,其中只含有的一种杂质是二氧化硅(二氧化硅不溶于水,不能与盐酸反应,高温下不发生分解反应).为了测定该石灰石的纯度,兴趣小组取用2g这种石灰石样品,用实验室现有的稀盐酸30g分次加入,充分反应后,经过滤、干燥等操作后称量,每次稀盐酸用量及剩余固体的质量见下表(利用实验数据绘制的图象如图所示)