题目内容
3.如图是氢氧化钙的溶解度曲线,30℃时,向0.5g氢氧化钙粉末加入100g水,充分搅拌后静置,下列说法正确的是( )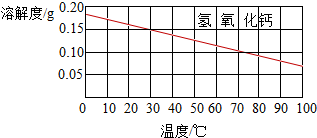
| A. | 所得溶液质量为100.5g | B. | 所得溶液是不饱和溶液 | ||
| C. | 降低温度溶液的质量变大 | D. | 升高温度溶液溶质质量分数变大 |
分析 A.根据30℃时氢氧化钙的溶解度解答;
B.根据30℃时氢氧化钙的溶解度解答;
C、根据氢氧化钙的溶解度曲线随温度变化情况解答;
D.根据氢氧化钙的溶解度随温度变化情况及溶质的质量分数解答.
解答 解:A.30℃时氢氧化钙的溶解度<0.15g,故30℃时,将0.5g氢氧化钙粉末加入到100g水中,充分搅拌不能完全溶解,所得溶液的质量小于100.5g,故错误;
B.30℃时氢氧化钙的溶解度<0.15g,故30℃时,将0.5g氢氧化钙粉末加入到100g水中,充分搅拌不能完全溶解,所得溶液是饱和溶液,故错误;
C.氢氧化钙的溶解度随温度升高而减小,故降低温度会继续溶解未溶的溶质,溶质的质量增加,溶剂的质量不变,所以降温溶液的质量变大,正确;
D.氢氧化钙的溶解度随温度升高而减小,故升高温度会析出溶质,溶质的质量减小,溶剂的质量不变,则溶质的质量分数变小,故说法错误;
故选:C.
点评 解答本题关键是能据物质的溶解度曲线分析溶液中各成分的变化情况,进而分析溶液的状态和溶质的质量分数的变化情况.

练习册系列答案
相关题目
4.如图是四个实验绘制的图象,其中实验结果与对应图象正确的是( )
| A. | 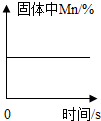 加热氯酸钾和二氧化锰的混合物 | |
| B. | 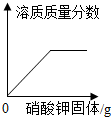 恒温下,在一定量的KNO3不饱和溶液中加入KNO3固体 | |
| C. | 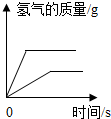 在等质量的镁、铁里分别加入足量的稀硫酸 | |
| D. | 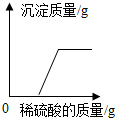 往一定量的NaOH和Ba(OH)2的混合溶液中加入稀硫酸至过量 |
11.氧气是我们身边最重要的物质,下列关于氧气的叙述正确的是( )
| A. | 氧化反应都是化合反应 | |
| B. | 水中生物的存活是由于氧气易溶于水 | |
| C. | 空气中氧气含量与健康无关 | |
| D. | 氧气可以供给呼吸,在体内发生缓慢氧化 |
18.敞口放置下列溶液,质量会增加的是( )
| A. | 氯化钠溶液 | B. | 浓硫酸 | C. | 浓盐酸 | D. | 食醋 |
15.请你参与实验室用生石灰制取氢氧化钠固体的研究.将一定量的生石灰加入一只洁净的烧杯中,加入碳酸钠溶液,充分反应后冷却到室温,通过过滤、洗涤、干燥得到固体A和溶液B,请回答以下问题.
【查阅资料】NaOH、Ca(OH)2的溶解度
(1)固体A中的成分是什么?
【猜想与假设】
甲同学认为是:CaCO3 乙同学认为是:CaCO3和Ca(OH)2
乙同学猜想可能含有Ca(OH)2的理由是氧化钙与水反应生成氢氧化钙.
【实验与探究】为了验证各自的猜想,甲、乙同学分别进行了实验:
【反思与评价】同学讨论后认为,甲同学的实验不能(填“能”或“不能”)证明固体A的成分,理由是加入稀盐酸有气泡只能证明有CaCO3,不能证明有无Ca(OH)2;
结合甲、乙两位同学的实验证明了乙同学的猜想是正确的,因此确定了固体A的成分.
(2)溶液B中溶质的成分是什么?
【猜想与假设】丙同学认为是:NaOH、Na2CO3
丁同学认为是:NaOH、Ca(OH)2
戊同学认为是:NaOH
【表达与交流】
①结合对固体成分的探究,同学们经过讨论确定了丁同学猜想正确,理由是因为固体中有Ca(OH)2,说明溶液为Ca(OH)2的饱和溶液;
②同学们欲将溶液B加热浓缩,加热不久,溶液出现浑浊,只好停止加热,请解释加热时溶液出现浑浊的原因是B溶液为Ca(OH)2的饱和溶液,加热,Ca(OH)2的溶解度随温度的升高而降低,故析出Ca(OH)2使溶液变浑浊.
【查阅资料】NaOH、Ca(OH)2的溶解度
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
| NaOH的溶解度(g/100g水) | 42 | 109 | 129 | 174 | 314 | 347 |
| Ca(OH)2的溶解度(g/100g水) | 0.18 | 0.16 | 0.14 | 0.12 | 0.09 | 0.07 |
【猜想与假设】
甲同学认为是:CaCO3 乙同学认为是:CaCO3和Ca(OH)2
乙同学猜想可能含有Ca(OH)2的理由是氧化钙与水反应生成氢氧化钙.
【实验与探究】为了验证各自的猜想,甲、乙同学分别进行了实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 甲同学:用一支洁净的试管取少量固体A,再加入过量稀盐酸. | 有气泡产生 | 自己的猜想 正确 |
| 乙同学:用一支洁净的试管取少量固体A,加水,充分振荡,向上层清液中滴加无色酚酞试液. | 上层清液由无色变为红色 | 自己的猜想 正确 |
结合甲、乙两位同学的实验证明了乙同学的猜想是正确的,因此确定了固体A的成分.
(2)溶液B中溶质的成分是什么?
【猜想与假设】丙同学认为是:NaOH、Na2CO3
丁同学认为是:NaOH、Ca(OH)2
戊同学认为是:NaOH
【表达与交流】
①结合对固体成分的探究,同学们经过讨论确定了丁同学猜想正确,理由是因为固体中有Ca(OH)2,说明溶液为Ca(OH)2的饱和溶液;
②同学们欲将溶液B加热浓缩,加热不久,溶液出现浑浊,只好停止加热,请解释加热时溶液出现浑浊的原因是B溶液为Ca(OH)2的饱和溶液,加热,Ca(OH)2的溶解度随温度的升高而降低,故析出Ca(OH)2使溶液变浑浊.

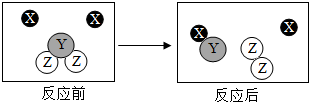 走进化学变化的微观世界,有利于进一步认识化学变化.如图是某化学变化的微观示意图,X、Y、Z分别表示不同类别的原子,据图回答问题:
走进化学变化的微观世界,有利于进一步认识化学变化.如图是某化学变化的微观示意图,X、Y、Z分别表示不同类别的原子,据图回答问题: