题目内容
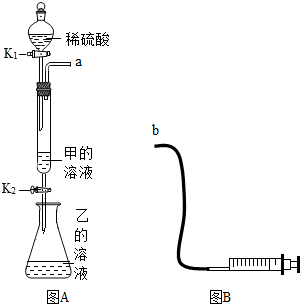
16.利用下列装置能达到相应实验目的是( )| A. | 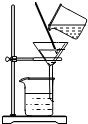 分离KNO3和NaCl | B. | 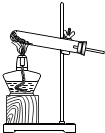 H2还原CuO | ||
| C. | 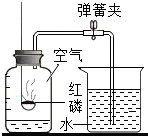 测定空气中O2的含量 | D. |  收集CO2气体 |
分析 A、根据过滤可以除去不溶于液体的固体;
B、根据氢气还原氧化铜的装置特点考虑;
C、根据红磷燃烧生成五氧化二磷,消耗了氧气考虑;
D、根据二氧化碳的密度考虑.
解答 解:A、由于硝酸钾和氯化钠都易溶于水,不能通过过滤分离,故A错;
B、氢气还原氧化铜时,导管要伸到试管的底部,试管口要去掉橡皮塞,故B错;
C、红磷燃烧生成五氧化二磷,消耗了氧气,使瓶内气压减小,所以水会进入瓶内,根据进入水的体积测定出消耗的氧气的体积,故C正确;
D、二氧化碳的密度比空气大,所以气体要从长管进,短管出,故D错.
故选C.
点评 解答本题关键是要知道过滤操作的目的,知道氢气还原氧化铜的注意事项,知道空气中氧气含量的测定方法,知道二氧化碳的收集方法.

练习册系列答案
相关题目
6.下列关于水的说法正确的是( )
| A. | 生活污水任意排放会污染环境 | B. | 水由氢分子和一个氧原子构成 | ||
| C. | 水是取之不尽,用之不竭的资源 | D. | 硬水经过滤可以转化为软水 |
 如图是A、B、C三种物质的溶解度曲线,据图回答:
如图是A、B、C三种物质的溶解度曲线,据图回答: 北京奥运让全世界兴奋,而在“水立方”中不断上演的狂破世界记录之举,泳池8天狂破19项世界纪录.伟大,水立方贡献了创造世界纪录的圣殿.令世人震惊--水立方到底有何种神奇的魔力,为各国运动员提供打破世界记录的舞台.当然,运动员们奋力拼搏是主要原因,此外,从建筑风水学来探索水立方中蕴涵的“秘密”,外层膜结构的封闭工程,充满魔幻色彩的建筑.
北京奥运让全世界兴奋,而在“水立方”中不断上演的狂破世界记录之举,泳池8天狂破19项世界纪录.伟大,水立方贡献了创造世界纪录的圣殿.令世人震惊--水立方到底有何种神奇的魔力,为各国运动员提供打破世界记录的舞台.当然,运动员们奋力拼搏是主要原因,此外,从建筑风水学来探索水立方中蕴涵的“秘密”,外层膜结构的封闭工程,充满魔幻色彩的建筑.