题目内容
6.有一种石灰干燥剂有效成份为氧化钙(CaO),在干燥吸水过程中发成如下反应CaO+H2O=Ca(OH)2,该干燥剂中氧化钙(CaO)的质量分数是80%,现有一包质量为70g的石灰干燥剂(不考虑杂质吸水).请计算:(1)70g的石灰干燥剂中含氧化钙(CaO)的质量.
(2)这包干燥剂理论上至少可以吸收水的质量.
分析 认真审题,找出已知量,然后根据化学方程式计算,就是依据反应物和生成物之间的质量比进行解答;注意单位正确使用.
解答 解:
(1)70g的石灰干燥剂中含氧化钙(CaO)的质量为70g×80%=56g
(2)设能够吸收水的质量为x,
CaO+H2O=Ca(OH)2
56 18
56g x
$\frac{56}{56g}=\frac{18}{x}$
x=18g
答案:
(1)70g的石灰干燥剂中含氧化钙(CaO)的质量为56g;
(2)这包干燥剂理论上至少可以吸收水的质量为18g.
点评 根据化学方程式的计算,必须对有关的化学知识有清晰的理解,熟练掌握有关反应的化学方程式.如果化学方程式中的化学式写错了,或者没有配平,化学计算必然会得出错误结果.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
14.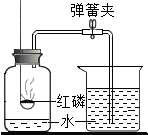 如图是实验室常用的测定空气中氧气含量的装置,下列对该实验认识正确的是( )
如图是实验室常用的测定空气中氧气含量的装置,下列对该实验认识正确的是( )
 如图是实验室常用的测定空气中氧气含量的装置,下列对该实验认识正确的是( )
如图是实验室常用的测定空气中氧气含量的装置,下列对该实验认识正确的是( )| A. | 该实验可用木炭代替 | |
| B. | 红磷燃烧产生大量白色气体 | |
| C. | 该实验可说明氮气不能为红磷助燃 | |
| D. | 红磷不足会导致测定的氧气含量偏大 |
1. 甲、乙两种物质的溶解度曲线如图所示.下列叙述正确的是( )
甲、乙两种物质的溶解度曲线如图所示.下列叙述正确的是( )
 甲、乙两种物质的溶解度曲线如图所示.下列叙述正确的是( )
甲、乙两种物质的溶解度曲线如图所示.下列叙述正确的是( )| A. | 依据溶解度曲线可判断,甲的溶解度比乙的大 | |
| B. | 将甲的饱和溶液变为不饱和溶液,可采取升温的方法 | |
| C. | 将甲、乙的饱和溶液从t2℃降到t1℃,甲的析出质量比乙的少 | |
| D. | t1℃时,甲和乙的溶液各100g,其溶质的质量一定相等 |
11.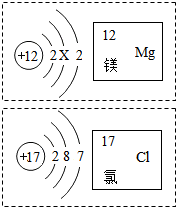 如图是镁和氯两种元素的有关信息,则下列说法错误的是( )
如图是镁和氯两种元素的有关信息,则下列说法错误的是( )
 如图是镁和氯两种元素的有关信息,则下列说法错误的是( )
如图是镁和氯两种元素的有关信息,则下列说法错误的是( )| A. | 镁原子结构图中X=8 | |
| B. | 氯元素的原子序数为17 | |
| C. | 镁是金属元素、氯是非金属元素 | |
| D. | 镁和氯组成的化合物氯化镁是混合物 |
15.下列实验操作正确的是( )
| A. |  | B. |  | C. |  | D. |  |
 A、B、C、D是初中化学常见的物质,它们分别属于氧化物、酸、碱或盐中的一种,相互反应的关系如图(“-”表示相连的两种物质能发生化学反应,“→”表示转化关系,部分反应物或生成物省略).其中A、B、C含有两种相同元素,B可用于改良酸性土壤.请按要求回答下列问题:
A、B、C、D是初中化学常见的物质,它们分别属于氧化物、酸、碱或盐中的一种,相互反应的关系如图(“-”表示相连的两种物质能发生化学反应,“→”表示转化关系,部分反应物或生成物省略).其中A、B、C含有两种相同元素,B可用于改良酸性土壤.请按要求回答下列问题: