题目内容
9.烟花爆竹的主要成分是黑火药,其化学组成为硝酸钾、硫磺和木炭等.(1)黑火药中至少有5种元素,欲分离出硝酸钾,可进行溶解、过滤、蒸发结晶等操作.
(2)黑火药的一般配方是:硫磺2g、硝酸钾3g、炭粉4.5g.已知黑火药在空气中燃爆时可发生:S+2KNO3+3C=K2S+3CO2↑+N2↑,则S、KNO3、C完全反应时的质量比为16:101:18,该配方中C和S(填化学式)明显过量.燃放烟花爆竹产生SO2的反应方程式是S+O2 $\frac{\underline{\;点燃\;}}{\;}$SO2.
(3)SO2气体在空气中经粉尘催化与氧气反应生成SO3;SO3与水反应,形成硫酸型酸雨,写出有关反应的化学方程式:2SO2+O2$\frac{\underline{\;催化剂\;}}{\;}$2SO3,SO3+H2O═H2SO4.
(4)很多城市出台”禁放“规定杜绝此类污染,以下解决”现代文明“与”传统文化“冲突的做法可行的是AB.(填字母)
A.提倡电子鞭炮 B.开发绿色鞭炮 C.关停鞭炮企业.
分析 (1)根据黑火药组成为硝酸钾、硫磺和木炭以及过滤可以除去不溶于水的物质进行解答;
(2)根据反应物和生成物及其质量守恒定律可以书写化学方程式;根据化学方程式可以判断反应物和生成物之间的质量比;
(3)SO2气体在空气中经粉尘催化氧化为SO3,SO3与水反应,写出反应的化学方程式即可;
(4)充分理解环境保护的重要性.
解答 解:(1)黑火药中至少有钾元素、氮元素、氧元素、碳元素、硫元素等5种元素.硫磺和碳不溶于水,硝酸钾易溶于水,可以用溶解、过滤、蒸发结晶等操作分离出硝酸钾.故填:5;溶解.
(2)S+2KNO3+3C=K2S+3CO2↑+N2↑,则S、KNO3、C完全反应时的质量比为:32:202:36=16:101:18.由反应物之间的质量比可知,碳和硫明显过量,燃放烟花爆竹产生SO2的反应方程式是:S+O2 $\frac{\underline{\;点燃\;}}{\;}$SO2.故填:16:101:18;S;S+O2 $\frac{\underline{\;点燃\;}}{\;}$SO2.
(3)SO2气体在空气中经粉尘催化氧化为SO3,SO3与水反应能生成硫酸,有关反应的化学方程式为:2SO2+O2$\frac{\underline{\;催化剂\;}}{\;}$2SO3;SO3+H2O═H2SO4.故填:2SO2+O2$\frac{\underline{\;催化剂\;}}{\;}$2SO3;SO3+H2O═H2SO4;
(4)提倡电子鞭炮、开发绿色鞭炮有利于环境保护,关停鞭炮企业是不现实的.故填:AB.
点评 解答本题要掌握化学方程式的书写方法和相关方面的计算方法,只有这样才能对问题做出正确的判断.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
17.某校化学兴趣小组同学测定大理石样品中碳酸钙的质量分数.准确称量20g大理石样品放入烧杯中,向烧杯中加入100mL过量的稀盐酸(杂质不反应),立即将烧杯放到电子秤上称量,记录数据如表.
(1)从表中可知,化学反应速度的变化趋势是越来越慢,原因是稀盐酸的质量分数越来越小.
(2)计算大理石样品中碳酸钙的质量分数(写出计算过程).
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 质量/g | 170.00 | 166.00 | 164.00 | 163.00 | 162.40 | 162.08 | 162.08 |
(2)计算大理石样品中碳酸钙的质量分数(写出计算过程).
1.镍氢充电电池有着广泛应用,镍及其化合物能发生下列反应:①Ni+2HCl=NiCl2+H2↑ ②NiO+2HCl=NiCl2+H2O ③NiO2+4HCl=NiCl2+Cl2↑+2H2O. Ni(OH)2不溶于水.对上述反应的分析判断错误的是( )
| A. | 镍能与氯化铜溶液发生置换反应 | |
| B. | 反应①是置换反应 | |
| C. | NiCl2能与NaOH溶液发生反应生成物中有沉淀 | |
| D. | 反应②中Ni的化合价发生了变化 |
18.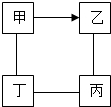 如图中“-”表示相连的物质间在一定条件下可以反应,“→”表示甲在一定条件下可以直接转化为乙.下面四组选项中,符合如图要求的是( )
如图中“-”表示相连的物质间在一定条件下可以反应,“→”表示甲在一定条件下可以直接转化为乙.下面四组选项中,符合如图要求的是( )
 如图中“-”表示相连的物质间在一定条件下可以反应,“→”表示甲在一定条件下可以直接转化为乙.下面四组选项中,符合如图要求的是( )
如图中“-”表示相连的物质间在一定条件下可以反应,“→”表示甲在一定条件下可以直接转化为乙.下面四组选项中,符合如图要求的是( ) | 甲 | 乙 | 丙 | 丁 | |
| A | H2SO4 | NaOH | NaCl | Na2CO3 |
| B | CO | CO2 | H2SO4 | CuO |
| C | Fe | Fe2(SO4)3 | Mg | HCl |
| D | O2 | CO | CuO | C |
| A. | A | B. | B | C. | C | D. | D |
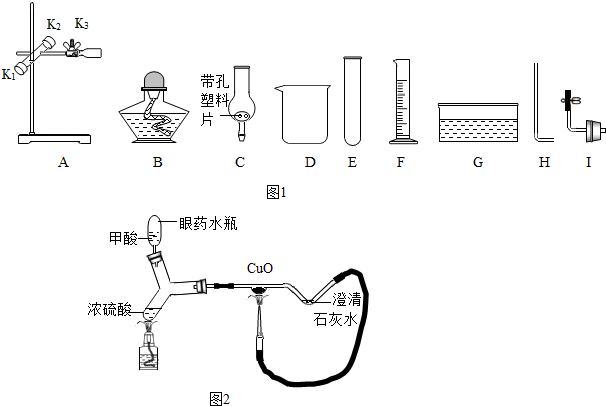

 多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界.
多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界.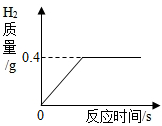 将一定质量的金属锌投入到100g稀硫酸中恰好完全反应,放出气体的质量与反应时间的关系如图所示,试求:
将一定质量的金属锌投入到100g稀硫酸中恰好完全反应,放出气体的质量与反应时间的关系如图所示,试求: