题目内容
6.要除去铜粉中混有的少量铁粉,下列物质不合适的是( )| A. | 稀硫酸 | B. | 稀盐酸 | C. | CuSO4溶液 | D. | NaOH溶液 |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、铁粉能与稀硫酸反应生成硫酸亚铁溶液和氢气,铜不与稀硫酸反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的试剂正确.
B、铁粉能与稀盐酸反应生成氯化亚铁溶液和氢气,铜不与稀盐酸反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的试剂正确.
C、铁粉能与CuSO4溶液反应生成氯化亚铁溶液和铜,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的试剂正确.
D、铁粉不与氢氧化钠溶液反应,不能把杂质除去,不符合除杂原则,故选项所采取的试剂错误.
故选:D.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
16.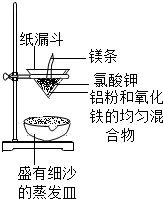 铝和氧化铁的反应:2A1+Fe2O3$\frac{\underline{\;900℃~1550℃\;}}{\;}$Al2O3+2Fe,称为“铝热反应”(如图所示),引燃镁条,漏斗内的物质熔化,镁条燃尽,漏斗下端仍持续产生大量熔融物落入沙中,该溶融物可用于焊接铁轨.
铝和氧化铁的反应:2A1+Fe2O3$\frac{\underline{\;900℃~1550℃\;}}{\;}$Al2O3+2Fe,称为“铝热反应”(如图所示),引燃镁条,漏斗内的物质熔化,镁条燃尽,漏斗下端仍持续产生大量熔融物落入沙中,该溶融物可用于焊接铁轨.
(1)实验中镁条的作用是给反应物加热;氧化铁和铝粉都用粉末状的,原因是增大接触面积,加快反应速率.
(2)某学习兴趣小组对所得熔融物的成分进行了探究.
【查阅资料】
①金属铝不但能和酸溶液(如稀盐酸)反应产生氢气,还能和强碱溶液(如氢氧化钠溶液)反应产生氢气.
②Al、A12O3、Fe、Fe2O3的熔点、沸点数据如下:
【实验猜想】
(3)某同学推测,铝热反应所得到的熔融物应是铁铝合金.理由是:该反应放热能使铁熔化,而铝的熔点比铁
低,此时液态的铁和铝熔合形成铁铝合金.你认为他的解释是否合理?合理(填“合理”或“不合理”).
(4)铝与稀盐酸反应的化学方程式为2Al+6HCl═2AlCl3+3H2↑.
(5)请你根据已有知识找出一种验证产物中有Fe的最简单的方法:把磁铁靠近产物,产物中固体能够被磁铁吸引,说明产物中含有铁.
【实验验证】
(6)设计一个简单的实验方案,证明上述所得的熔融物中含有金属铝,请填写下列表格:
 铝和氧化铁的反应:2A1+Fe2O3$\frac{\underline{\;900℃~1550℃\;}}{\;}$Al2O3+2Fe,称为“铝热反应”(如图所示),引燃镁条,漏斗内的物质熔化,镁条燃尽,漏斗下端仍持续产生大量熔融物落入沙中,该溶融物可用于焊接铁轨.
铝和氧化铁的反应:2A1+Fe2O3$\frac{\underline{\;900℃~1550℃\;}}{\;}$Al2O3+2Fe,称为“铝热反应”(如图所示),引燃镁条,漏斗内的物质熔化,镁条燃尽,漏斗下端仍持续产生大量熔融物落入沙中,该溶融物可用于焊接铁轨.(1)实验中镁条的作用是给反应物加热;氧化铁和铝粉都用粉末状的,原因是增大接触面积,加快反应速率.
(2)某学习兴趣小组对所得熔融物的成分进行了探究.
【查阅资料】
①金属铝不但能和酸溶液(如稀盐酸)反应产生氢气,还能和强碱溶液(如氢氧化钠溶液)反应产生氢气.
②Al、A12O3、Fe、Fe2O3的熔点、沸点数据如下:
| 物质 | A1 | Al2O3 | Fe | Fe203 |
| 熔点/℃ | 660 | 2054 | 1535 | 1462 |
| 沸点/℃ | 2467 | 2980 | 2750 | - |
(3)某同学推测,铝热反应所得到的熔融物应是铁铝合金.理由是:该反应放热能使铁熔化,而铝的熔点比铁
低,此时液态的铁和铝熔合形成铁铝合金.你认为他的解释是否合理?合理(填“合理”或“不合理”).
(4)铝与稀盐酸反应的化学方程式为2Al+6HCl═2AlCl3+3H2↑.
(5)请你根据已有知识找出一种验证产物中有Fe的最简单的方法:把磁铁靠近产物,产物中固体能够被磁铁吸引,说明产物中含有铁.
【实验验证】
(6)设计一个简单的实验方案,证明上述所得的熔融物中含有金属铝,请填写下列表格:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量冷却后的熔融物于试管中,加入氢氧化钠溶液 | 产生气泡 | 熔融物中含有铝 |
14.下列物质中,由原子构成的是( )
| A. | 水银 | B. | 水 | C. | 液氧 | D. | 氯化钠 |
1.完全中和某硫酸溶液,需要一定质量的氢氧化钠,若改用相同质量的氢氧化钙,反应后溶液( )
| A. | pH>7 | B. | pH<7 | ||
| C. | pH=7 | D. | 可使紫色石蕊试液变红 |
15.下列反应中属于化合反应的是( )
| A. | Fe+H2SO4=FeSO4+H2↑ | B. | Na2O+H2O=2NaOH | ||
| C. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | D. | BaCl2+Na2SO4=BaSO4↓+2NaCl |
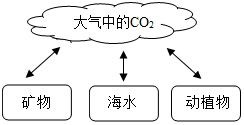 图是自然界碳的循环示意图,请据图分析后回答:
图是自然界碳的循环示意图,请据图分析后回答: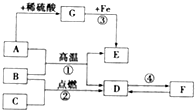 如图A~G是初中化学常见的物质,其中A为黑色固体,E为红色固体单质,B、C、D均为无色气体,F为石灰石的主要成分,G是蓝色溶液,请根据如图回答下列问题:
如图A~G是初中化学常见的物质,其中A为黑色固体,E为红色固体单质,B、C、D均为无色气体,F为石灰石的主要成分,G是蓝色溶液,请根据如图回答下列问题: