题目内容
分析下面1-18号元素原子结构示意图.
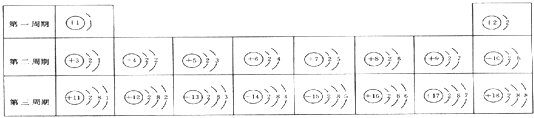
(1)这是元素周期表的一部分,是科学家______发现并编制的.从表中看出决定元素种类的是______.
(2)在化学反应中,第一纵行的元素比较容易______电子;第六、七纵行的元素比较容易______电子,可见元素的化学性质主要决定于原子的______数.
(3)同一周期有许多规律,如(写一条)______.
(4)某粒子的结构示意图为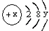 ,当x-y=8时,该粒子符号为______.
,当x-y=8时,该粒子符号为______.
解:(1)元素周期表的一部分,是科学家 门捷列夫发现并编制的.元素是具有相同核电荷数即质子数的一类原子的总称,故决定元素种类的是 质子数(或核电荷数).
(2)由原子结构示意图可以看出,在化学反应中,第一纵行的元素原子最外层有一个电子,比较容易 失电子;第六、七纵行的元素原子最外层电子数多于4个,比较容易 得电子,可见元素的化学性质主要决定于原子的 最外层电子数.
(3)由元素周期表及原子结构示意图可以看出同一周期的元素电子层数相同(或最外层电子数1-8递增或核电荷数依次递增).
(4)某粒子的结构示意图为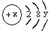 ,x-y=8,即y=x-8;由此时可以看出核内质子数x,核外电子数为x+2,核外电子数比核内质子数多2,则依据形成离子的特点,故x=16,y=8,粒子符号为 S2-.
,x-y=8,即y=x-8;由此时可以看出核内质子数x,核外电子数为x+2,核外电子数比核内质子数多2,则依据形成离子的特点,故x=16,y=8,粒子符号为 S2-.
故答案为:(1)门捷列夫质子数(或核电荷数).
(2)失 得 最外层电子.
(3)电子层数相同(或最外层电子数1-8递增或核电荷数依次递增).
(4)S2-.
分析:(1)根据元素的定义分析.
(2)根据原子结构示意图最外层电子数分析.
(3)根据同一周期原子结构示意图特点分析.
(4)根据粒子结构示意图结构特点分析.
点评:本题考查了原子的结构示意图的意义,培养学生分析信息寻找规律以及解决问题的能力.
(2)由原子结构示意图可以看出,在化学反应中,第一纵行的元素原子最外层有一个电子,比较容易 失电子;第六、七纵行的元素原子最外层电子数多于4个,比较容易 得电子,可见元素的化学性质主要决定于原子的 最外层电子数.
(3)由元素周期表及原子结构示意图可以看出同一周期的元素电子层数相同(或最外层电子数1-8递增或核电荷数依次递增).
(4)某粒子的结构示意图为
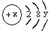 ,x-y=8,即y=x-8;由此时可以看出核内质子数x,核外电子数为x+2,核外电子数比核内质子数多2,则依据形成离子的特点,故x=16,y=8,粒子符号为 S2-.
,x-y=8,即y=x-8;由此时可以看出核内质子数x,核外电子数为x+2,核外电子数比核内质子数多2,则依据形成离子的特点,故x=16,y=8,粒子符号为 S2-.故答案为:(1)门捷列夫质子数(或核电荷数).
(2)失 得 最外层电子.
(3)电子层数相同(或最外层电子数1-8递增或核电荷数依次递增).
(4)S2-.
分析:(1)根据元素的定义分析.
(2)根据原子结构示意图最外层电子数分析.
(3)根据同一周期原子结构示意图特点分析.
(4)根据粒子结构示意图结构特点分析.
点评:本题考查了原子的结构示意图的意义,培养学生分析信息寻找规律以及解决问题的能力.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
下列对有关主题知识的归纳完全正确的一组是
| A. 安全常识 | B. 物质用途 |
| 化学实验室:严禁烟火 熄灭酒精灯:用嘴吹灭酒精灯 | 液态氢:火箭的燃料 液态氮:医疗手术 |
| C.物质的制取 | D.元素与人体健康 |
| 汽油:在催化剂作用下分解水获得 氧气:用分离液态空气法获得 | 缺碘:会导致甲状腺疾病 缺铁:会导致贫血 |
- A.A
- B.B
- C.C
- D.D
 竹子是“有节、中空、四季常绿”的植物(如图所示).同学们对竹子中的气体成分展开了探究,测定其成分.
竹子是“有节、中空、四季常绿”的植物(如图所示).同学们对竹子中的气体成分展开了探究,测定其成分.
(1)收集竹子中的气体.
小华提出:将一节竹子浸没在水中,在竹子上钻孔,用排水法收集气体.
小刚提出:可用注射器从竹子中抽取气体.
大家认为两人的想法都可行,于是分为A、B两组,在相同条件下,A组采用小华的取气方法,B组采用小刚的取气方法,分别完成下面的实验.
(2)检验气体中是否含有二氧化碳气体.
| 实验步骤 | 实验现象 | 实验结论及解释 |
| 向所取得气体中加入 ① | ② | 有二氧化碳 |
【查阅资料】红磷的着火点为240℃,白磷的着火点为40℃.
【设计实验】同学们设计了如下图所示的方案一和方案二来测定氧气含量.

【进行实验】按上述两个方案进行多次实验.
【反思与评价】
a.实验中磷的量应为足量,原因是______.
b.两个方案的实验测定结果不同,测定结果比较准确的是方案______,原因是______
______
c.经过A、B两组同学的实验,A组测得的含氧量总是大于B组的,你认为原因是______.
某纺织厂为了除去棉麻原料中的非纤维素,可用一定溶质的质量分数的碳酸钠溶液煮沸棉麻原料.现需要80kg20%的碳酸钠溶液.
(1)若用碳酸钠固体和水配制上述溶液,需要碳酸钠的质量是______kg;水的质量是______kg.
(2)甲乙两组同学分别用不同的方案,探究所配得的溶液中碳酸钠的质量分数是否为20%,设计并完成了以下实验:
| 甲组 | 乙组 | |||||||||||||||||
| 实验过程 | I.取质量是100g的三个烧杯,各盛20g所配得的碳酸钠溶液. II.向三个烧杯中分别放入溶质质量分数相同,但溶液质量不同的盐酸溶液; III.充分反应后再分别称量烧杯及剩余溶液; | I.取质量是100g的一个烧杯,盛20g所配得的碳酸钠溶液. II.向三个烧杯中滴入溶质质量分数为20%的氯化钙溶液,直到不再产生沉淀为止,过滤、洗涤、晾干、称重; III.绘制加入氯化钙溶液与产生沉淀的质量关系如下图; | ||||||||||||||||
| 所得的数据或关系图 |
| 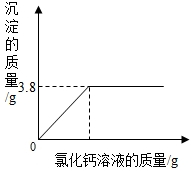 已知发生反应的化学方程式为: Na2CO3+CaCl2═CaCO3↓+2NaCl |
①甲组实验1中产生气体的质量是______g;
②依据甲乙两组的数据分别计算所配得的溶液中碳酸钠的质量分数;
甲:______; 乙:______.(精确到0.1%)
测定结果与20%之间产生差异可能是实验原理、操作过程等因素引起的.