题目内容
15. 金属材料是工农业生产和人们生活离不开的材料之一,人类每年要从自然界获取大量的金属材料资源.根据对金属和金属材料的认识,回答:
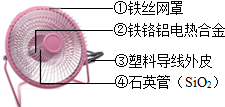
金属材料是工农业生产和人们生活离不开的材料之一,人类每年要从自然界获取大量的金属材料资源.根据对金属和金属材料的认识,回答:(1)如图所示的小型取暖器(俗称小太阳)的主要制作材料中,属于金属材料的是①②(填序号).
(2)颗粒达到纳米级的单质铁具有很强的反应活性,俗称“纳米铁”.实验室制备的方法是:以高纯氮气作保护气,在高温条件下用H2和FeCl2发生置换反应,生成“纳米铁”.该反应的化学方程式为FeCl2+H2$\frac{\underline{\;高温\;}}{\;}$Fe+2HCl.
(3)若将一定量的铁粉投入到一定量只含有Cu(NO3)2、AgNO3的工业废水中,充分反应后过滤,向所得滤渣中滴加稀盐酸,无气泡产生,则滤渣中一定含有的金属是Ag;滤液中一定含有的金属离子是Fe2+.
分析 (1)根据材料的分类进行解答;
(2)根据反应物和产物以及反应条件书写化学方程式;
(3)由金属活动顺序铁粉能与废水中的Cu(NO3)2、AgNO3都能发生反应,所以在滤渣中可能含有金属铜和银;根据题意可知,滤渣中一定不含铁粉,“充分反应”后铁粉可能量不足而未能与废水中Cu(NO3)2反应但一定与废水中的AgNO3发生反应,工业废水中的AgNO3一定被置换生成金属银.而铁粉是否与废水中的Cu(NO3)2发生反应,因铁粉量不足而无法确定.
解答 解:
(1)金属材料包含金属和合金,所以属于金属材料的是铁丝网罩、铁铬铝电热合金,而属于有机合成材料的是塑料,石英管是无机非金属材料;
(2)在高温条件下用H2和FeCl2发生置换反应,生成铁和氯化氢,化学方程式为:FeCl2+H2$\frac{\underline{\;高温\;}}{\;}$Fe+2HCl;
(3)根据上述分析,工业废水中的AgNO3一定被置换生成金属银;“充分反应”后铁粉被完全反应掉,滤渣中一定不含铁粉;铁粉是否与废水中的Cu(NO3)2发生反应,因铁粉量不足而无法确定.则滤渣中一定含有金属银,一定不含金属铁,可能含有金属铜.滤液中一定含有的金属离子是铁粉与盐溶液反应生成的 Fe2+.
答案:
(1)铁丝网罩、铁铬铝电热合金;
(2)FeCl2+H2$\frac{\underline{\;高温\;}}{\;}$Fe+2HCl;
(3)Ag; Fe2+.
点评 本题主要考查基础知识,较为简单.根据金属活动性顺序,结合题中实验现象,分析反应的发生,判断反应后所得固体的组成.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.2015年10月,诺贝尔生理学或医学奖被授予中国科学家屠呦呦,以表彰她发现了治疗疟疾的药物--青蒿素.下列关于青蒿素(化学式C15H22O5)说法错误的是( )
| A. | 青蒿素是由碳、氢、氧三种元素组成的 | |
| B. | 青蒿素是由15个碳原子、22个氢原子、5个氧原子构成的 | |
| C. | 青蒿素中碳元素质量分数最大 | |
| D. | 青蒿素中氢、氧原子的个数比为22:5 |
10.归纳推理是学习化学的重要方法之一.下列有关事实的推理,结论合理的是( )
| A. | H2O和CO2都不能使紫色石蕊变红,把它们混合在一起时却能够使石蕊变红,说明CO2与H2O发生了化学反应 | |
| B. | 在“测定空气中氧气含量”的实验中,集气瓶内水平面上升约1/5,证明了氧气约占空气总质量的1/5 | |
| C. | Al制品的耐腐蚀性比Cu制品强,因此Al的活泼性小于铜 | |
| D. | 盐中含有金属离子和酸根离子,而NH4NO3中没有金属离子,所以不属于盐 |
20.下列符号中既可以表示一种元素,又可以表示一种物质的是( )
| A. | Fe | B. | H | C. | N2 | D. | O2- |
7. 如图所示是一改进后的电解水装置,下列说法正确的是( )
如图所示是一改进后的电解水装置,下列说法正确的是( )
 如图所示是一改进后的电解水装置,下列说法正确的是( )
如图所示是一改进后的电解水装置,下列说法正确的是( )| A. | 检查该装置气密性时,可以先关闭两边的活塞,向中间的漏斗中加水,形成一段水柱后静置,若水面不下降,说明气密性良好 | |
| B. | b为电源的正极 | |
| C. | 管①做如图改进后,有利于用带火星的木条检验该气体 | |
| D. | 该实验说明了水是由氢气和氧气组成的 |
4.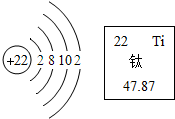 如图是钛元素的原子结构示意图和钛元素在元素周期表中的单元格,下列说法错误的是( )
如图是钛元素的原子结构示意图和钛元素在元素周期表中的单元格,下列说法错误的是( )
 如图是钛元素的原子结构示意图和钛元素在元素周期表中的单元格,下列说法错误的是( )
如图是钛元素的原子结构示意图和钛元素在元素周期表中的单元格,下列说法错误的是( )| A. | 钛属于金属元素 | |
| B. | 钛的核电荷数为22 | |
| C. | 钛的相对原子质量为47.87g | |
| D. | 在化学反应中,钛原子容易得到电子 |
11.青少年一定不要吸烟,香烟的烟气中危害最大的物质是尼古丁(化学式为:C10H14N2),下列关于尼古丁的说法错误的是( )
| A. | 尼古丁的相对分子质量是162 | |
| B. | 尼古丁由C、H、N三种元素组成 | |
| C. | 尼古丁由10个碳原子、14个氢原子和1个氮分子构成 | |
| D. | 尼古丁中碳、氢、氮元素质量之比为60:7:14 |
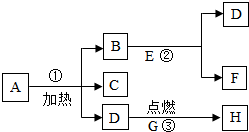 A、B…H八种物质,有如图所示关系:其中D能使带火星的木条复燃,H是一种能使澄清石灰水变浑浊的气体,在②的反应前后B的质量和化学性质都不改变:
A、B…H八种物质,有如图所示关系:其中D能使带火星的木条复燃,H是一种能使澄清石灰水变浑浊的气体,在②的反应前后B的质量和化学性质都不改变: