题目内容
16.某实验小组的同学用氢氧化钡溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钡溶液加入一定量稀盐酸后,发现忘记了滴加指示剂.因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究.【提出问题】该烧杯内溶液中的溶质是什么?
【猜想与假设】猜想一:BaCl2和Ba(OH)2;
猜想二:①BaCl2;
猜想三:BaCl2和HCl.
【实验探究】实验一:取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡.观察到②无明显变化(或溶液颜色不变),得出结论:猜想一不成立;
实验二:取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量,开始时有气泡产生,继续滴加一段时间后出现白色沉淀,得出结论:猜想二不成立,猜想三成立.
【表达与交流】实验二中,产生上述现象的原因是③滴加碳酸钠先跟稀盐酸反应,生成二氧化碳,有气泡产生,待稀盐酸耗尽后,碳酸钠与氯化钡反应,生成碳酸钡白色沉淀;
【反思与拓展】
(1)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑④可溶性反应物的剩余;
(2)要处理烧杯内的溶液,使其溶质只含有BaCl2,应向烧杯中加入过量的⑤碳酸钡.
分析 根据反应的程度进行猜想:恰好反应、一种物质完全反应,另一种物质有剩余;
根据酚酞遇碱变红来进行解答;
据碳酸钠与盐酸和氯化钡反应的现象解答;
根据实验的结论进行发生反思;
根据盐酸的性质进行分析,但注意不能引进其它的金属离子.
解答 解:猜想二:反应可能是恰好反应,只有氯化钡;也可能是一种物质完全反应,另一种物质有剩余,若氢氧化钡过量,则含有氢氧化钡和氯化钡;若盐酸过量,则含有盐酸和氯化钡;
【实验探究】因为酚酞遇碱会变红色,而结论是猜想一不正确,即不含有氢氧化钡,故观察到的现象是溶液不变红色;
【表达与交流】取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量,盐酸与碳酸钠反应产生气泡,盐酸消耗掉后,氯化钡再与碳酸钠反应产生沉淀;
【反思与拓展】(1)因为反应可能是完全反应,也可能是其中的一种反应物过量,因此在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物的用量;
(2)除去溶液中的盐酸可用适量的碳酸钡,碳酸钙和盐酸反应生成氯化钡、水和二氧化碳.
故答案为:①BaCl2;②无明显变化(或溶液颜色不变);③滴加碳酸钠先跟稀盐酸反应,生成二氧化碳,有气泡产生,待稀盐酸耗尽后,碳酸钠与氯化钡反应,生成碳酸钡白色沉淀;④可溶性反应物的剩余;⑤碳酸钡.
点评 本题考查了酸碱中和反应以及实验设计的能力.设计实验时,可以从反应后的产物和其有关的性质着手.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.属于溶液的是( )
| A. | 豆浆 | B. | 牛奶 | C. | 矿泉水 | D. | 蒸馏水 |
4.氢氧化钠是重要的工业原料,以下是有关它的性质实验.
①图1反应的化学反应方程式为NaOH+HCl=NaCl+H2O,反应后溶液(编号为a)中溶质的组成情况可能有3种.为证明溶液a中可能含有的溶质,进行了如下实验.
Ⅰ.确定溶液a中是否含有氢氧化钠
Ⅱ.确定溶液a中是否含有盐酸
i.上述方案中有一个设计不合理,指出不合理的实验方案编号及原因方案一不合理,生成的氯化钠也会与硝酸银生成白色沉淀;
ii.采取正确的实验方案,进行实验,根据现象得到的结论是溶液中含有稀盐酸,且溶质是氯化钠和氯化氢;
Ⅲ.欲从溶液a中得到纯净的氯化钠,可以采取的实验操作是蒸发结晶.
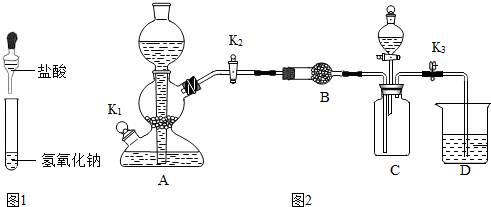
②利用如图2装置验证氢氧化钠能与二氧化碳反应.(装置气密性良好)
Ⅰ装置A用于制取二氧化碳,打开k2、k3,当D中紫色石蕊试液变红色,可确定C中收集满二氧化碳.
Ⅱ.装置B中的药品是无水硫酸铜,用于干燥二氧化碳,写出该反应的化学反应方程式CuSO4+5H2O=CuSO4•5H2O.
Ⅲ.C中收集满二氧化碳后,使A中反应暂停的操作是关闭K2.
IV.甲同学打开装置C中分液漏斗活塞,将8mL室温时氢氧化钠饱和溶液滴入C中,然后关闭活塞,观察到D中石蕊试液倒流至C中.甲同学得出结论,氢氧化钠能与二氧化碳反应.
Ⅴ.乙同学认为上述现象不足以证明氢氧化钠能与二氧化碳发生反应,还应利用上述装置补充一个对比实验.
结论:氢氧化钠能与二氧化碳反应,写出该反应的化学反应方程式2NaOH+CO2=Na2CO3+H2O.
①图1反应的化学反应方程式为NaOH+HCl=NaCl+H2O,反应后溶液(编号为a)中溶质的组成情况可能有3种.为证明溶液a中可能含有的溶质,进行了如下实验.
Ⅰ.确定溶液a中是否含有氢氧化钠
| 步骤 | 现象 | 结论 |
| 取少量溶液a,滴加氯化铜溶液 | (26)溶液中无蓝色絮状沉淀 | 不含氢氧化钠 |
| 方案 | 步骤 | 现象 |
| 一 | 取少量溶液a,滴加硝酸银溶液 | 产生白色沉淀 |
| 二 | 取少量溶液a,加入镁粉 | 产生气泡 |
ii.采取正确的实验方案,进行实验,根据现象得到的结论是溶液中含有稀盐酸,且溶质是氯化钠和氯化氢;
Ⅲ.欲从溶液a中得到纯净的氯化钠,可以采取的实验操作是蒸发结晶.
②利用如图2装置验证氢氧化钠能与二氧化碳反应.(装置气密性良好)
Ⅰ装置A用于制取二氧化碳,打开k2、k3,当D中紫色石蕊试液变红色,可确定C中收集满二氧化碳.
Ⅱ.装置B中的药品是无水硫酸铜,用于干燥二氧化碳,写出该反应的化学反应方程式CuSO4+5H2O=CuSO4•5H2O.
Ⅲ.C中收集满二氧化碳后,使A中反应暂停的操作是关闭K2.
IV.甲同学打开装置C中分液漏斗活塞,将8mL室温时氢氧化钠饱和溶液滴入C中,然后关闭活塞,观察到D中石蕊试液倒流至C中.甲同学得出结论,氢氧化钠能与二氧化碳反应.
Ⅴ.乙同学认为上述现象不足以证明氢氧化钠能与二氧化碳发生反应,还应利用上述装置补充一个对比实验.
| 液体 | 步骤 | 现象 |
| 水 | 打开分液漏斗活塞,加入液体后关闭活塞 | D中导管现有气泡冒出,后D中导管无明显现象 |

1.归纳推理是学习化学的重要方法之一.下列有关事实的推理,结论合理的是( )
| 事实 | 结论 | |
| A | 在“测定空气中氧气含量”的实验中,集气 瓶内水平面上升约$\frac{1}{5}$ | 氧气约占空气总质量的$\frac{1}{5}$ |
| B | 白磷和红磷均是由磷元素组成的单质 | 白磷和红磷属于同一种物质 |
| C | H2O和CO2都不能使紫色石蕊变红,但 把它们混合在一起时却能够使石蕊变红 | CO2与H2O发生了化学反应 |
| D | Al制品的耐腐蚀性比Cu制品强 | Al的活泼性小于铜 |
| A. | A | B. | B | C. | C | D. | D |
8.下列化学用语与对应表述不相符的是( )
| A. | Fe2+-铁离子 | |
| B. | 2H-2个氢原子 | |
| C. | 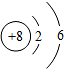 -氧原子的结构示意图 -氧原子的结构示意图 | |
| D. | $\stackrel{+2}{Mg}$O-氧化镁中镁元素的化合价为+2价 |
5.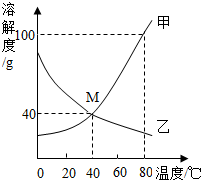 如图是甲、乙两种物质的溶解度曲线,下列有关说法中不正确的是( )
如图是甲、乙两种物质的溶解度曲线,下列有关说法中不正确的是( )
 如图是甲、乙两种物质的溶解度曲线,下列有关说法中不正确的是( )
如图是甲、乙两种物质的溶解度曲线,下列有关说法中不正确的是( )| A. | 升高温度可将乙物质的饱和溶液转化为不饱和溶液 | |
| B. | M点的含义是40℃时甲乙两物质的溶解度相等且为40g | |
| C. | 80℃时,甲物质饱和溶液中溶质的质量分数为50% | |
| D. | 若甲物质中混有少量的乙,可用降温结晶的方法来提纯甲物质 |
6.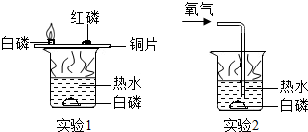 如图是一组用于研究可燃物燃烧条件的对比实验,对有关实验现象和结论的判断不正确的是( )
如图是一组用于研究可燃物燃烧条件的对比实验,对有关实验现象和结论的判断不正确的是( )
 如图是一组用于研究可燃物燃烧条件的对比实验,对有关实验现象和结论的判断不正确的是( )
如图是一组用于研究可燃物燃烧条件的对比实验,对有关实验现象和结论的判断不正确的是( )| A. | 可燃物燃烧需要氧气(或空气),并达到着火点 | |
| B. | 实验1中红磷未燃烧,说明红磷的着火点高于白磷 | |
| C. | 实验2中如果停止通入氧气,燃着的白磷会熄灭 | |
| D. | 实验2中白磷燃烧,说明实验2中的热水温度高于实验1 |
 2013年12月14日,“嫦娥三号”在月球虹湾成功着陆.
2013年12月14日,“嫦娥三号”在月球虹湾成功着陆.