题目内容
16. 阅读下面科普短文.
阅读下面科普短文.锂电池是指电极材料含金属锂或含锂化合物、使用非水溶液做离子导体的电池.最早出现的锂电池利用化学反应Li+MnO2LiMnO2提供电能.银白色的金属锂是所有金属中最轻的一种,它的化学性质活泼,常温下就能和空气中的氧气化合成氧化锂;锂还能和水剧烈反应变成氢氧化锂(LiOH),同时放出一种可燃性气体.
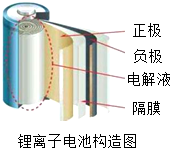
随着科技的发展,锂电池的应用范围逐步扩大,一类新型锂电池--锂离子电池大量应用在手机、笔记本电脑和家用小电器上.锂离子电池由正极、负极、隔膜和电解液构成,正极材料(如石墨)和负极材料(如LiCoO2)均能传导电子,电解液在正、负两极之间起输运离子、传导电流的作用.锂离子电池采用一种类似摇椅式的工作原理,充放电过程中锂离子在正负极间来回穿梭,从一边“摇”到另一边,往复循环,实现电池的充放电过程.由于锂离子电池中包含的电解液多含有机物,普遍存在易燃问题,在过充、过放、短路及热冲击等滥用的状态下,电池温度迅速升高,常常会导致电池起火,甚至爆炸.因此,目前大多数数码产品都会配备相应的保护元件,当检测到电池到达满电状态,会自动切断充电电路.
依据文章内容,回答下列问题:
(1)锂电池放电时,将化学反应释放的能量转化成电能.
(2)锂离子电池由正极、负极、薄膜和电解液构成.
(3)锂离子电池的正极材料采用石墨是利用了其导电的物理性质.
(4)锂电池使用非水溶液做离子导体的原因是2Li+2H2O═2LiOH+H2↑.(用化学方程式表示)
(5)安全使用锂离子电池的措施有避免过充.
分析 (1)根据电池的原理进行分析;
(2)根据锂离子电池的构成解答;
(3)根据石墨具有导电性解答;
(4)根据锂和水反应生成氢氧化锂和氢气解答;
(5)根据安全使用锂离子电池的措施解答》
解答 解:(1)电池就是将化学能转化为电能的装置;
(2)锂离子电池由正极、负极、薄膜和电解液 构成;
(3)石墨具有导电性,锂离子电池的正极材料采用石墨是利用了其导电的物理性质;
(4)锂和水反应生成氢氧化锂和氢气,反应的化学方程式为:2Li+2H2O═2LiOH+H2↑;
(5)安全使用锂离子电池的措施有:避免过充(或避免过放、短路、热冲击等;使用保护软件等).
答案:
(1)电;(2)正极、负极、薄膜和电解液;(3)导电;
(4)2Li+2H2O═2LiOH+H2↑;(5)避免过充.
点评 本题考查较为综合,涉及原电池的涉及,金属的腐蚀及防护以及新型化学电源,题目难度中等,注意有关基础知识的积累.

练习册系列答案
相关题目
8.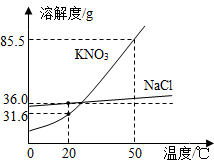 如图为NaCl、KNO3的溶解度曲线.下列说法不正确的是( )
如图为NaCl、KNO3的溶解度曲线.下列说法不正确的是( )
 如图为NaCl、KNO3的溶解度曲线.下列说法不正确的是( )
如图为NaCl、KNO3的溶解度曲线.下列说法不正确的是( )| A. | 20℃时,100g水中加入32g KNO3,溶液中KNO3的质量分数$\frac{32g}{100g+32g}$×100%为 | |
| B. | 下列实验中的X、Y、Z三种溶液,属于饱和溶液的是Y 100g水$→_{搅拌(20℃)}^{加25gKNO_{3}}$X$→_{搅拌(20℃)}^{加25gKNO_{3}}$Y$→_{至50℃}^{升温}$Z | |
| C. | 欲使NaCl溶液由不饱和变为饱和,可采用加NaCl或蒸发水的方法 | |
| D. | 除去KNO3固体中混有的少量NaCl,实验步骤是溶解、蒸发浓缩、降温结晶、过滤 |
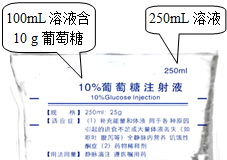 因病不能进食者,可以通过点滴葡萄糖、脂肪乳等为人体提供所需能量.
因病不能进食者,可以通过点滴葡萄糖、脂肪乳等为人体提供所需能量. “合理膳食,均衡营养”会让我们更健康.
“合理膳食,均衡营养”会让我们更健康.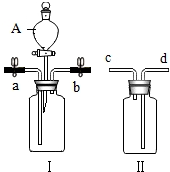 利用如图装置进行有关物质性质的实验.
利用如图装置进行有关物质性质的实验.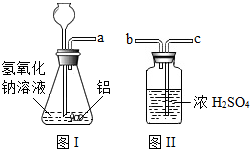 实验中,小红误将氢氧化钠溶液当成酸滴加到装有金属锌的试管中,结果发现也有气泡产生,为了解该气体的成分,实验小组进行了一下探究活动:
实验中,小红误将氢氧化钠溶液当成酸滴加到装有金属锌的试管中,结果发现也有气泡产生,为了解该气体的成分,实验小组进行了一下探究活动: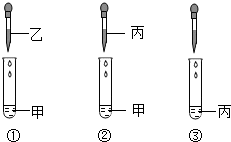 甲、乙、丙、丁都是初中化学中最常见的物质,已知它们由H、O、C、Cl、Na、Ca 6种元素中的2种或3种组成,丙与甲、乙、丁都能发生反应.将这四种物质的溶液按图所示相互滴加,现象为:①产生白色沉淀;②有气泡冒出;③无明显现象
甲、乙、丙、丁都是初中化学中最常见的物质,已知它们由H、O、C、Cl、Na、Ca 6种元素中的2种或3种组成,丙与甲、乙、丁都能发生反应.将这四种物质的溶液按图所示相互滴加,现象为:①产生白色沉淀;②有气泡冒出;③无明显现象