题目内容
10.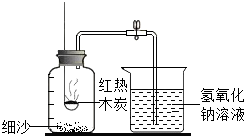 某研究性学习小组在“利用燃碳法测定空气中氧气的体积分数”的实验时(如图装置),发现一个现象:氢氧化钠溶液吸收生成的二氧化碳后,进入集气瓶中氢氧化钠溶液的体积分数仍然小于$\frac{1}{5}$.
某研究性学习小组在“利用燃碳法测定空气中氧气的体积分数”的实验时(如图装置),发现一个现象:氢氧化钠溶液吸收生成的二氧化碳后,进入集气瓶中氢氧化钠溶液的体积分数仍然小于$\frac{1}{5}$.(1)写出氢氧化钠溶液吸收二氧化碳发生反应的化学方程式CO2+2NaOH=Na2CO3+H2O.
(2)教材中利用燃烧红磷法测定空气中氧气体积分数,选择该药品的原因是红磷只能与氧气反应且生成物为固体.
【提出问题】是什么原因导致测量不准确呢?
【猜想与假设】他们分别作了如下猜想:
甲同学:可能是木炭取的量过少;
乙同学:可能是木炭燃烧没有消耗完集气瓶中的氧气;
小组同学发现实验结束后,燃烧匙中还有残留的黑色固体,都认为甲同学的猜想不合理.
【查阅资料】木炭、棉花和蜡烛在密闭容器内燃烧停止后,残留氧气的体积分数高达14.0%、8.0%和16.0%.
乙同学又利用上述装置设计了如下实验,请你填写下表.
| 实验步骤 | 实验现象 | 实验结论 |
| 1将足量木炭点燃,迅速插入集气瓶中 | 棉花继续燃烧 | 木炭燃烧没有消耗完集气瓶中的氧气. |
| 2待冷却后,将燃着的棉花(填“棉花”或“蜡烛”)再伸入该集气瓶中 |
(3)请分析步骤2中,你选择的可燃物的理由三种物质燃烧时需要的氧气浓度大小依次为蜡烛>木炭>棉花.
(4)由此实验你对物质燃烧的条件有何新的认识可燃物燃烧需要的氧气要达到一定的浓度(或可燃物燃烧需要足够的氧气).
(5)从木炭燃烧反应的产物分析你认为测量结果小于$\frac{1}{5}$的理由还有可能是木炭燃烧生成了CO.
分析 (1)根据氢氧化钠溶液与二氧化碳反应生成碳酸钠和水解答;
(2)根据用燃烧红磷法测定空气中氧气体积分数的原理解答;
【查阅资料】根据题中信息和燃烧的条件分析解答;
【交流与反思】
(3)根据三种物质燃烧时需要的氧气浓度大小解答;
(4)根据可燃物燃烧需要的氧气要达到一定的浓度(或可燃物燃烧需要足够的氧气)解答;
(5)根据木炭完全燃烧生成二氧化碳,不完全燃烧生成一氧化碳解答.
解答 解:(1)氢氧化钠溶液与二氧化碳反应生成碳酸钠和水,发生反应的化学方程式为:CO2+2NaOH=Na2CO3+H2O;
(2)教材中利用燃烧红磷法测定空气中氧气体积分数,红磷燃烧生成五氧化二磷固体,故选择该药品的原因是红磷只能与氧气反应且生成物为固体;
【查阅资料】
将足量木炭点燃,迅速插入集气瓶中,待冷却后,将燃着的棉花再伸入该集气瓶中,棉花继续燃烧,说明集气瓶中有氧气,木炭燃烧没有消耗完集气瓶中的氧气;
【交流与反思】
(3)三种物质燃烧时需要的氧气浓度大小依次为蜡烛>木炭>棉花,故选棉花;
(4)由此实验可以知道:可燃物燃烧需要的氧气要达到一定的浓度(或可燃物燃烧需要足够的氧气);
(5)木炭完全燃烧生成二氧化碳,不完全燃烧生成一氧化碳,从木炭燃烧反应的产物分析你认为测量结果小于$\frac{1}{5}$的理由还有可能是木炭燃烧生成了CO.
答案:
(1)CO2+2NaOH=Na2CO3+H2O;
(2)红磷只能与氧气反应且生成物为固体.
【查阅资料】
| 实验步骤 | 实验现象 | 实验结论 |
| 棉花 | 棉花继续燃烧 |
(3)三种物质燃烧时需要的氧气浓度大小依次为蜡烛>木炭>棉花;
(4)可燃物燃烧需要的氧气要达到一定的浓度(或可燃物燃烧需要足够的氧气);
(5)木炭燃烧生成了CO.
点评 本考点考查了空气中氧气的含量的探究,并且注重了实验方案的评价,对实验方案进行评价是近几年中考的一个重点.评价包括对实验方案的评价、实验过程的评价、实验结论的评价等,要认真把握.

练习册系列答案
 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
5.日前科学家发现了一种新型二维半导体材料一氧化锡(SnO),该发现有望将电子设备速度提高100倍.下列关于一氧化锡的说法正确的是( )
| A. | 它是混合物 | |
| B. | 它的分子静止不动 | |
| C. | 它的分子之间不再有间隔 | |
| D. | 它的一个分子由1个氧原子和1个锡原子构成 |
15.推理是学习化学的重要方法,下列推理正确的是( )
| A. | 根据组成物质的元素种类,可将纯净物分为单质和化合物 | |
| B. | 原子形成离子时,电子层数一定减少 | |
| C. | 同种元素的原子具有相同的质子数,因此质子数相同的微粒一定属于同种元素 | |
| D. | 木炭、硫磺、红磷和铁丝燃烧都是化合反应,因此物质的燃烧一定属于化合反应 |
2.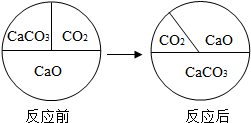 如图表示三种物质在密闭容器中反应前后质量比例的变化,下列说法正确的是( )
如图表示三种物质在密闭容器中反应前后质量比例的变化,下列说法正确的是( )
 如图表示三种物质在密闭容器中反应前后质量比例的变化,下列说法正确的是( )
如图表示三种物质在密闭容器中反应前后质量比例的变化,下列说法正确的是( )| A. | 该反应是化合反应 | B. | 该反应中CO2是生成物 | ||
| C. | 该反应中CaO起催化作用 | D. | 该反应是分解反应 |
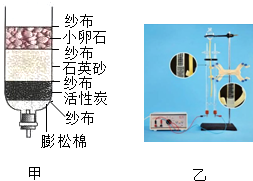 2016年3月22日是“世界水日”,水与人类的生活和生产密切相关.
2016年3月22日是“世界水日”,水与人类的生活和生产密切相关.