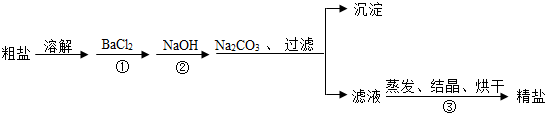
题目内容
4.在天平两端的烧杯中盛有等质量,等质量分数的盐酸,天平平衡.分别向一只烧杯中加入一定质量的镁,另一只烧杯中加入一定质量的铝,充分反应后,天平仍然平衡,则加入Mg和Al的质量比可能是( )| A. | 11:12 | B. | 32:33 | C. | 3:4 | D. | 1:1 |
分析 天平仍然平衡,说明溶液增加的质量相等,据此可得出本题的答案.
解答 解:第一种情况:两者都恰好完全反应:
设镁的质量为x,铝的质量为y,溶液增加的质量为z.
Mg+2HCl=MgCl2+H2↑ 增加的质量
24 2 24-2=22
x z
$\frac{24}{x}=\frac{22}{z}$
x=$\frac{24z}{22}$
2Al+6HCl=2AlCl3+3H2↑ 增加的质量
54 6 54-6=48
y z
$\frac{54}{y}=\frac{48}{z}$
y=$\frac{54z}{48}$
加入镁和铝的质量比为:$\frac{24z}{22}=\frac{54z}{48}$=32:33.故选B
第二种情况,金属过量:
则生成氢气与盐酸质量有关,会相等,所以加入的金属质量是相等的.故选D.
故选B、D.
点评 本题主要考查有关化学方程式的计算,难度较大.关键是要将溶液增加的质量作为得到答案的桥梁.题目没有说明金属必须是相等等条件,所以存在各种可能性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.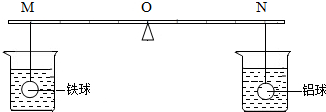 在杠杆的两端分别挂着质量和体积都相同的铁球和铝球,这时杠杆平衡.将两球分别浸没在质量相同、溶质的质量分数也相同的稀硫酸中(如图),直至两个烧杯中均没有气泡产生为止.两球的外形变化不大且无孔洞出现.下列推测中,正确的是( )
在杠杆的两端分别挂着质量和体积都相同的铁球和铝球,这时杠杆平衡.将两球分别浸没在质量相同、溶质的质量分数也相同的稀硫酸中(如图),直至两个烧杯中均没有气泡产生为止.两球的外形变化不大且无孔洞出现.下列推测中,正确的是( )
 在杠杆的两端分别挂着质量和体积都相同的铁球和铝球,这时杠杆平衡.将两球分别浸没在质量相同、溶质的质量分数也相同的稀硫酸中(如图),直至两个烧杯中均没有气泡产生为止.两球的外形变化不大且无孔洞出现.下列推测中,正确的是( )
在杠杆的两端分别挂着质量和体积都相同的铁球和铝球,这时杠杆平衡.将两球分别浸没在质量相同、溶质的质量分数也相同的稀硫酸中(如图),直至两个烧杯中均没有气泡产生为止.两球的外形变化不大且无孔洞出现.下列推测中,正确的是( )| A. | 左端产生的氢气比右端的少 | |
| B. | 反应结束后要使杠杆平衡,支点应向N移动(液体体积变化忽略不计) | |
| C. | 拿掉烧杯后,杠杆仍然平衡(金属球上附着的液体忽略不计,下同) | |
| D. | 拿掉烧杯后,要想使杠杆平衡,支点应向M移动 |
15.根据金属活动性顺序判断,组内物质间能够发生化学反应的是( )
| A. | 铜和稀盐酸 | B. | 铁和硫酸锌溶液 | C. | 银和稀硫酸 | D. | 锌和硝酸银溶液 |
13.酸、碱、盐是几类重要的化合物,他们之间能发生复分解反应.
(1)复分解反应发生的条件是有沉淀析出,或有气体放出,或有水生成.
(2)某化学小组进行“酸和碱的中和反应”实验:将盐酸滴入一定量的澄清石灰水中,实验无明显现象.取反应后的部分溶液加热、蒸干、得到白色固体.
以下是探究白色固体成分的实验,已知CaCl2溶液呈中性.请填写表:
实验反思:无明显现象的中和反应可借助酸碱指示剂判断反应终点.
(1)复分解反应发生的条件是有沉淀析出,或有气体放出,或有水生成.
(2)某化学小组进行“酸和碱的中和反应”实验:将盐酸滴入一定量的澄清石灰水中,实验无明显现象.取反应后的部分溶液加热、蒸干、得到白色固体.
以下是探究白色固体成分的实验,已知CaCl2溶液呈中性.请填写表:
| 实验操作 | 测定结果 | 白色固体成分 |
| 用pH试纸测定反应后溶液的酸碱度,操作方法是用洁净玻璃棒蘸取溶液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较. | pH>7 | |
| CaCl2 |
14.如图所示实验基本操作不正确的是( )
| A. | 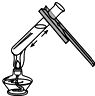 给盛有液体的试管加热 | B. |  向试管中加入液体 | ||
| C. |  闻药品气味 | D. | 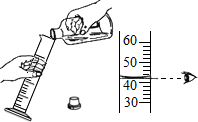 量取液体体积 |