题目内容
14.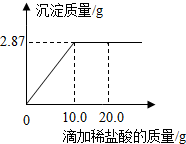 为测定某AgNO3溶液的溶质质量分数,用溶质质量分数为7.3%的稀盐酸进行滴定.现取待测液50.0g,滴定过程如图所示.(滴定反应为:AgNO3+HCl═AgCl↓+HNO3,计算结果均保留1位小数)
为测定某AgNO3溶液的溶质质量分数,用溶质质量分数为7.3%的稀盐酸进行滴定.现取待测液50.0g,滴定过程如图所示.(滴定反应为:AgNO3+HCl═AgCl↓+HNO3,计算结果均保留1位小数)(1)AgNO3溶液的溶质质量为3.4g;
(2)计算恰好完全反应时,所得溶液的溶质质量分数.
分析 硝酸银和稀盐酸反应生成白色沉淀氯化银和硝酸,根据反应的化学方程式和图中通过的数据可以进行相关方面的计算.
解答 解:(1)设硝酸银的质量为x,反应生成硝酸质量为y,
由图中信息可知,反应生成氯化银沉淀的质量是2.87g,
HCl+AgNO3═AgCl↓+HNO3,
170 143.5 63
x 2.87g y
$\frac{170}{x}$=$\frac{143.5}{2.87g}$=$\frac{63}{y}$,
x=3.4g,y=1.26g,
故填:3.4.
(2)恰好完全反应时消耗10.0g稀盐酸,所得溶液的溶质质量分数为:$\frac{1.26g}{50.0g+10.0g-2.87g}$×100%=2.2%,
答:恰好完全反应时消耗10.0g稀盐酸,所得溶液的溶质质量分数为2.2%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.

练习册系列答案
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
5.下列说法正确的是( )
| A. | 用甲醛溶液浸泡海产品保鲜 | |
| B. | 用氢氧化钠溶液去除氧气中少量水蒸气 | |
| C. | 熟石灰能与稀盐酸反应,因此熟石灰用于治疗胃酸过多 | |
| D. | 鉴别羊毛与合成纤维,在空气中点燃,闻产生的气味 |
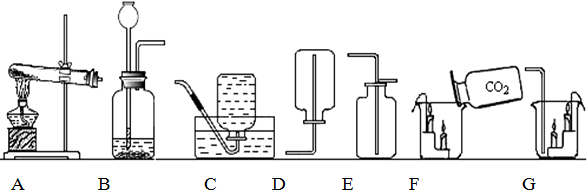
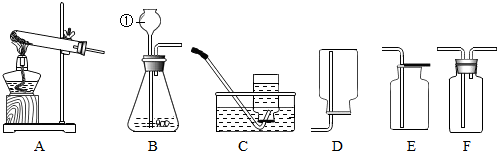
2.下列装置所示的实验中,能达到实验目的是( )
| A. | 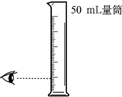 量取9.3mL稀盐酸 | B. | 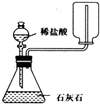 制取并收集CO2气体 | ||
| C. | 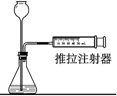 检查装置气密性 | D. | 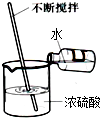 浓硫酸的稀释 |
6.下列方案合理的是( )
| A. | 验证碱能与酸反应:将H2SO4溶液滴入Cu(OH)2中 | |
| B. | 检验碳酸根离子:将要检验的物质与稀盐酸混合,观察是否产生气泡 | |
| C. | 验证质量守恒定律:将锌粒与稀硫酸混合,比较混合前后溶液的质量 | |
| D. | 鉴别H2、CH4、CO三种气体:分别将燃着的木条伸入集气瓶内,观察现象 |
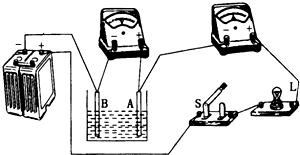 如图所示,A、B为两个电极,放在盛有稀硫酸的玻璃容器内.闭合开关后,A电极上出现的气泡为氧气,B电极上出现的气泡为氢气,在这一过程中,电流表示数逐渐变变大;灯泡亮度逐渐变亮.
如图所示,A、B为两个电极,放在盛有稀硫酸的玻璃容器内.闭合开关后,A电极上出现的气泡为氧气,B电极上出现的气泡为氢气,在这一过程中,电流表示数逐渐变变大;灯泡亮度逐渐变亮.
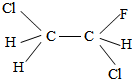 央视二套(这是真的吗?)栏目播出了电脑浸在液体中也能正常工作的新鲜事,这种液体可为手机电脑“洗澡”,用来清洗电子产品,它是被称作“绝缘液”的一氟二氯乙烷,结构如图,下列说法正确的是C.
央视二套(这是真的吗?)栏目播出了电脑浸在液体中也能正常工作的新鲜事,这种液体可为手机电脑“洗澡”,用来清洗电子产品,它是被称作“绝缘液”的一氟二氯乙烷,结构如图,下列说法正确的是C.