题目内容
8.家庭中常用洁厕剂的有效成分是盐酸,小明同学想测定某品牌洁厕剂中氯化氢的质量分数.他将足量的石灰石加入洁厕剂样品中(石灰石中的杂质既不与酸反应,也不溶于水),有关实验数据见表:| 反应前 | 反应后 | ||
| 实验数据 | 洁厕剂样品的质量 | 加入石灰石的质量 | 剩余物的总质量 |
| 73g | 50g | 114.2g | |
(1)反应后生成二氧化碳的质量为8.8g.
(2)该洁厕剂中氯化氢的质量分数.
分析 石灰石的主要成分碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,由质量守恒定律,混合物减少的质量即生成的二氧化碳质量,据此根据反应的化学方程式列式计算出参加反应的稀盐酸中溶质的质量,进而计算出该洁厕剂中氯化氢的质量分数.
解答 解:(1)反应后生成二氧化碳的质量为73g+50g-114.2g=8.8g.
(2)设参加反应的稀盐酸中溶质的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
73 44
x 8.8g
$\frac{73}{44}=\frac{x}{8.8g}$ x=14.6g
该洁厕剂中氯化氢的质量分数为$\frac{14.6g}{73g}$×100%=20%.
答:(1)8.8g;(2)该洁厕剂中氯化氢的质量分数为20%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,根据质量守恒定律计算出二氧化碳的质量是正确解答本题的前提和关键.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
5.下列方法不能达到实验目的是( )
| A. | 用水区分烧碱和硝酸铵两种固体 | |
| B. | 用硝酸银溶液区分氯化钠和氯化钙溶液 | |
| C. | 除去氧化铜中含有的铜粉:在空气中加热 | |
| D. | 除去二氧化碳中含有的水蒸气,将气体通过浓硫酸 |
6.下列化学用语表达正确的是( )
| A. | 氯酸钾中氯元素的化合价:K$\stackrel{+3}{Cl}$O3 | |
| B. | 镁离子的结构示意图: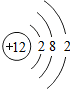 | |
| C. | 两个乙醇分子:2C2H5OH | |
| D. | 工业上炼铁的主要反应原理:3C+2Fe2O3$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑ |
16.下列化学符号与含义相符的是( )
| A. | Fe2+:1个铁离子 | B. | 3O:3个氧分子 | ||
| C. | 2OH-:2个氢氧根离子 | D. | N2:2个氮原子 |
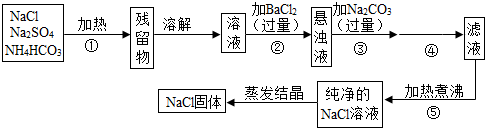
 如图“五连环”中的每一环表示一种物质,在一定条件下,相连环物质间能发生反应,不相连环物质间不能发生反应.已知A、B、C、D分别是铁、氧气、二氧化碳、氯化钡溶液、氢氧化钠溶液中的一种物质.若A为氧气,则D的化学式为( )
如图“五连环”中的每一环表示一种物质,在一定条件下,相连环物质间能发生反应,不相连环物质间不能发生反应.已知A、B、C、D分别是铁、氧气、二氧化碳、氯化钡溶液、氢氧化钠溶液中的一种物质.若A为氧气,则D的化学式为( )