题目内容
18.把铁和铜的混合物样品22.4克投入到100克的稀硫酸中恰好反应,生成0.4克氢气(1)求混合物中铜的质量分数
(2)反应后所得溶液的质量分数
(3)所用硫酸的质量分数是多少?
分析 铁与稀硫酸反应生成硫酸亚铁溶液和氢气,由生成氢气的质量,由反应的化学方程式列式计算出参加反应的铁的质量、稀硫酸中溶质的质量、生成的硫酸亚铁的质量,进而计算出混合物中铜的质量分数、反应后所得溶液的质量分数、所用硫酸的质量分数即可.
解答 解:设参加反应的铁的质量为x,生成的硫酸亚铁的质量为y,稀硫酸中溶质的质量为z,
Fe+H2SO4═FeSO4+H2↑
56 98 152 2
x z y 0.4g
(1)$\frac{56}{2}=\frac{x}{0.4g}$ x=11.2g
混合物中铜的质量分数为$\frac{22.4g-11.2g}{22.4g}$×100%=50%.
(2)$\frac{152}{2}=\frac{y}{0.4g}$ y=30.4g
反应后所得溶液的质量分数为$\frac{30.4g}{11.2g+100g-0.4g}$×100%≈27.4%.
(3)$\frac{98}{2}=\frac{z}{0.4g}$ z=19.6g
所用硫酸的质量分数是$\frac{19.6g}{100g}$×100%=19.6%.
答:(1)混合物中铜的质量分数为50%;
(2)反应后所得溶液的质量分数为27.4%;
(3)所用硫酸的质量分数是19.6%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
8.下列实验现象描述正确的是( )
| A. | 一氧化碳燃烧,放出热量,火焰呈蓝色 | |
| B. | 铜丝插入硫酸铝溶液中,溶液由无色变为蓝色 | |
| C. | 点燃棉线,会闻到烧焦羽毛的气味 | |
| D. | 硫在氧气中燃烧,发出蓝紫色火焰,放出热量 |
9.下列有关实验室制取气体的说法错误的是( )
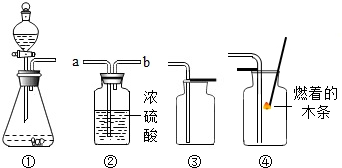

| A. | 装置①可作为CO2的发生装置 | B. | 装置④是收集CO2气体的验满方法 | ||
| C. | 装置③可用作O2的收集装置 | D. | 装置②干燥O2时,气体由a管进b管出 |
14.根据金属活动性顺序分析,下列描述或判断正确的是( )
| A. | 金属钾能与硫酸锌溶液发生化学反应得到金属锌 | |
| B. | 把金属铁加入硝酸银和硝酸铜溶液中,金属铁先与硝酸银发生反应 | |
| C. | 在常温下,铝比镁更容易与氧气发生化学反应 | |
| D. | 金属铜与氯化银反应得到金属银 |
15.把一定质量的甲、乙、丙、丁四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下表.下列说法不正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前的质量(g) | 4.0 | 2.0 | 3.0 | 2.0 |
| 反应后的质量(g) | 1.2 | x | 2.4 | 5.4 |
| A. | X=2.0,乙可能是催化剂 | B. | 甲和丙是反应物 | ||
| C. | 丁一定是化合物 | D. | 参加反应的甲、丙质量比是1:2 |
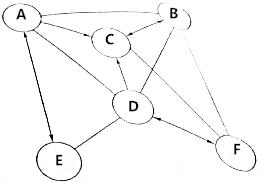 A、B、C、D、E、F是碳酸钠溶液、稀盐酸、氢氧化钙溶液、二氧化碳,一种氧化物和一种未知溶液,用连线表示能反应,箭头表示可以转化.试回答问题.
A、B、C、D、E、F是碳酸钠溶液、稀盐酸、氢氧化钙溶液、二氧化碳,一种氧化物和一种未知溶液,用连线表示能反应,箭头表示可以转化.试回答问题.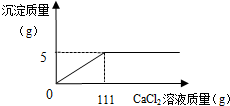 某碳酸钠和氯化钠的混合粉末21.2g,不断加入CaCl2溶液,产生沉淀的质量与所加入的CaCl2溶液的关系如图所示.
某碳酸钠和氯化钠的混合粉末21.2g,不断加入CaCl2溶液,产生沉淀的质量与所加入的CaCl2溶液的关系如图所示.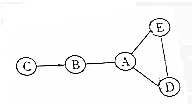 已知A、B、C、D、E均为初中化学常见的物质,相互关系如图所示,“→”表示转化关系,“-”表示相互之间反应(部分反应物、生成物以及反应条件省略).其中A是人体胃酸的主要成分,C是一种常用的食品干燥剂,与水反应放出大量的热,E是地壳中含量居第二位的金属元素组成的单质,请回答:
已知A、B、C、D、E均为初中化学常见的物质,相互关系如图所示,“→”表示转化关系,“-”表示相互之间反应(部分反应物、生成物以及反应条件省略).其中A是人体胃酸的主要成分,C是一种常用的食品干燥剂,与水反应放出大量的热,E是地壳中含量居第二位的金属元素组成的单质,请回答: