题目内容
3.红磷在氧气中燃烧,生成物是五氧化二磷.在该反应中反应的红磷、氧气、五氧化二磷的质量比是( )| A. | 4:5:2 | B. | 31:32:142 | C. | 31:32:64 | D. | 124:160:284 |
分析 根据红磷在氧气中燃烧生成五氧化二磷的化学方程式,计算反应中三种物质的质量比.
解答 解:方法一:基本解法,红磷在氧气中燃烧生成五氧化二磷的化学方程式为:4P+5O2 $\frac{\underline{\;点燃\;}}{\;}$ 2P2O5
该反应中磷、氧气、五氧化二磷的质量比=(4×31):(5×16×2):[2×(31×2+16×5)]=124:160:284
方法二:利用质量守恒定律的技巧解法,根据质量质量守恒定律,反应物质量和与生成物质量和应相等,因此质量比中反应物磷、氧气的和等于生成物五氧化二磷的量,则只有选项D中满足124+160=284;
故选D.
点评 根据反应的化学方程式,反应中各物质的质量比为各物质相对分子(或原子)质量与反应中物质计量数乘积的比.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.丙氨酸(C3H7NO2)是构成蛋白质的基本单位.下列有关丙氨酸的说法错误的是( )
| A. | 是一种氧化物 | |
| B. | 碳和氢两种元素的质量比为36﹕7 | |
| C. | 丙氨酸分子由13个原子构成 | |
| D. | 分子中碳氢氮氧四种原子的个数比为3﹕7﹕1﹕2 |
8.下列说法错误的是( )
| A. | 最外层电子数为8的粒子不一定是稀有气体元素的原子 | |
| B. | 含氧的化合物不一定是氧化物 | |
| C. | 软水中一定不含可溶性钙、镁离子的化合物 | |
| D. | 常用肥皂水可简易区分硬水与软水 |
15.下列物质的性质中,属于物质化学性质的是( )
| A. | 氧气不易溶于水 | B. | 一氧化碳具有还原性 | ||
| C. | 铁具有延展性 | D. | 汽油易挥发 |
12.下列解释没有体现水的主要作用的是( )
| A | B | C | D | |
| 实 验 装 置 | 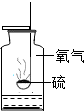 硫在氧气中燃烧 |  测定空气中氧气含量 |  铁丝在氧气中燃烧 |  探究燃烧的条件 |
| 解释 | 集气瓶中的水:吸收放出的热量 | 量筒中的水:通过水体积的变化得出O2体积 | 集气瓶中的水:冷却溅落融熔物,防止集气瓶炸裂 | 烧杯中的水:加热铜 片;隔绝空气 |
| A. | A | B. | B | C. | C | D. | D |
 化学用语是学习化学的重要工具,按要求用适当的化学用语填空:
化学用语是学习化学的重要工具,按要求用适当的化学用语填空: 在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小明很感兴趣,于是,他和同学们进行探究.
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小明很感兴趣,于是,他和同学们进行探究.