题目内容
1.要配制5L24.5%的硫酸溶液(密度为1.22g/ml),需要98%的浓硫酸(密度为1.84g/ml)多少毫升?需加水多少毫升?分析 根据溶液稀释前后溶质的质量不变,溶质质量=溶液质量×溶质的质量分数,结合题意进行分析解答.
解答 解:设需要98%的浓硫酸的体积为x,根据溶液稀释前后溶质的质量不变,5L=5000mL,
则1.84g/mL×x×98%=1.22g/mL×5000mL×24.5% x≈828.8mL.
需要加水的质量为1.22g/mL×5000mL-1.84g/mL×828.8mL≈4575g(合4575mL).
答:需要98%的浓硫酸(密度为1.84g/ml)828.8mL,需加水4575mL.
点评 本题难度不大,考查溶液的稀释问题,掌握溶液稀释前后溶质的质量不变是正确解答此类题的关键所在.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
11.黑火药是我国四大发明之一,黑火药的爆炸可用以下式子表示其反应物和生成物:2KNO3+3C+S$\frac{\underline{\;点燃\;}}{\;}$K2S+N2+3X,则X的化学式为( )
| A. | NO2 | B. | SO2 | C. | CO2 | D. | H2O |
9.下列情况可能引起空气污染的是 ( )
①煤和石油的燃烧②工业废气的任意排放③燃放鞭炮④飞机汽车尾气的排放. ⑤人体呼出的气体.
①煤和石油的燃烧②工业废气的任意排放③燃放鞭炮④飞机汽车尾气的排放. ⑤人体呼出的气体.
| A. | 只有①② | B. | 只有③④ | C. | ①②③④⑤ | D. | ①②③④ |
6.在常温下硫酸的密度与溶质的质量分数对照表如下:
(1)由上表可以看出的规律是常温下硫酸的密度随着溶质的质量分数的增大而增大
(2)实验室要用98%的浓硫酸配制20%的稀硫酸250mL,需98%的浓硫酸多少毫升?需再加水的体积是多少?
| 密度/g/cm3 | 1.07 | 1.14 | 1.30 | 1.50 | 1.73 | 1.84 |
| 溶质质量分数/ | 10 | 20 | 40 | 60 | 80 | 98 |
(2)实验室要用98%的浓硫酸配制20%的稀硫酸250mL,需98%的浓硫酸多少毫升?需再加水的体积是多少?
4.下列有关实验现象描述错误的是( )
| A. | 红磷在空气中燃烧产生大量白烟 | |
| B. | 硫在氧气中燃烧产生淡蓝色火焰 | |
| C. | 铁丝在氧气中剧烈燃烧,火星四射,生成一种黑色固体 | |
| D. | 木炭在氧气中剧烈燃烧,发白光 |
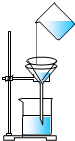 指出如图所示过滤操作中的错误地方
指出如图所示过滤操作中的错误地方