题目内容
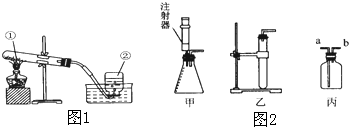
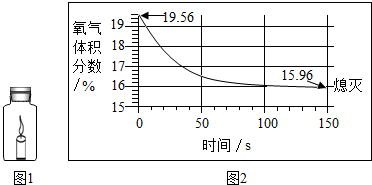
蜡烛(足量)在如图1所示的密闭容器内燃烧至熄灭,用仪器测出这一过程中瓶内氧气含量的变化(如图2所示).下列判断中,不正确的是( )

| A、瓶中氧气浓度小于一定值时,蜡烛无法燃烧 |
| B、实验过程中瓶中二氧化碳的含量增大 |
| C、该过程中瓶内物质总质量不变 |
| D、蜡烛熄灭原因是瓶内没有了氧气 |
考点:蜡烛燃烧实验
专题:结合课本知识的信息
分析:根据已有的知识结合图示进行分析,反应前氧气的体积分数是19.56%,当氧气的体积分数达到15.96%时,蜡烛熄灭,说明开始时瓶内含有其他气体,氧气的浓度低于一定值时,蜡烛无法燃烧,蜡烛燃烧生成二氧化碳和水,任何化学反应都遵循质量守恒定律.
解答:解:A.当氧气的体积分数达到15.96%时,蜡烛熄灭,说明氧气的浓度低于一定值时,蜡烛无法燃烧,故正确;
B.蜡烛燃烧生成二氧化碳,所以瓶中二氧化碳的含量增大了,故正确;
C.任何化学反应都遵循质量守恒定律,密闭容器内的物质的质量不会改变,故正确;
D.当氧气的体积分数达到15.96%时,蜡烛熄灭,说明此时瓶内仍有氧气,故错误.
故选D.
B.蜡烛燃烧生成二氧化碳,所以瓶中二氧化碳的含量增大了,故正确;
C.任何化学反应都遵循质量守恒定律,密闭容器内的物质的质量不会改变,故正确;
D.当氧气的体积分数达到15.96%时,蜡烛熄灭,说明此时瓶内仍有氧气,故错误.
故选D.
点评:本题考查了蜡烛的燃烧,完成此题,可以依据蜡烛燃烧的实质结合图示进行.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
关于KNO3的描述不正确的是(相对原子质量 O:16 K:39 N:14 )( )
| A、KNO3是一种复合肥料 |
| B、KNO3中氮元素的化合价为+3价 |
| C、KNO3中钾元素与氧元素的质量比为39:48 |
| D、KNO3由钾离子和硝酸根离子构成 |
某K2CO3样品,可能含有Na2CO3、MgCO3、NaCl中的几种杂质.取该样品6.9g,加入50g稀盐酸中,恰好完全反应得到无色溶液,同时产生2.2g气体.下列判断正确的是( )
| A、样品中一定没有MgCO3 |
| B、NaCl不与盐酸反应,说明样品中一定没有NaCl |
| C、所加稀盐酸中溶质的质量分数为7.3% |
| D、Na2CO3和MgCO3都能和稀盐酸反应生成气体,说明样品中一定有Na2CO3和MgCO3 |
下列物质中属于盐的是( )
| A、AgCl |
| B、H3PO4 |
| C、Fe3O4 |
| D、Zn(OH)2 |
海南椰粉含有丰富的“钙、铁、锌”,这里的“钙、铁、锌”应理解为( )
| A、单质 | B、原子 | C、分子 | D、元素 |
 材料:2013年12月2日,“嫦娥三号”探测器由长征三号运载火箭发射,首次实现月球软着陆和月面巡视勘察.12月15日晚,“嫦娥三号”着陆器和巡视器(玉兔月球车)成功分离,顺利互拍,任务取得圆满成功.长征三号运载火箭主要用于发射地球同步轨道有效载荷,它的一子级和二子级使用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作推进剂,三子级则使用效能更高的液氢(H2)和液氧(O2).
材料:2013年12月2日,“嫦娥三号”探测器由长征三号运载火箭发射,首次实现月球软着陆和月面巡视勘察.12月15日晚,“嫦娥三号”着陆器和巡视器(玉兔月球车)成功分离,顺利互拍,任务取得圆满成功.长征三号运载火箭主要用于发射地球同步轨道有效载荷,它的一子级和二子级使用偏二甲肼(C2H8N2)和四氧化二氮(N2O4)作推进剂,三子级则使用效能更高的液氢(H2)和液氧(O2).