题目内容
2.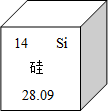 在元素周期表中,硅元素的某些信息如图所示,下列有关硅的说法错误的是( )
在元素周期表中,硅元素的某些信息如图所示,下列有关硅的说法错误的是( )| A. | 原子序数为14 | B. | 元素符号为Si | ||
| C. | 属于金属元素 | D. | 相对原子质量为28.09 |
分析 根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析判断即可.
解答 解:A.根据元素周期表中的一格中获取的信息,该元素的原子序数为14,故选项说法正确.
B.根据元素周期表中的一格中获取的信息,该元素的元素符号是Si,故选项说法正确.
C.根据元素周期表中的一格中获取的信息,该元素的名称是硅,属于非金属元素,故选项说法错误.
D.根据元素周期表中的一格中获取的信息,可知元素的相对原子质量为28.09,故选项说法正确.
故选C.
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息及辨别元素种类的方法进行分析解题的能力.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
12.加碘食盐中碘元素以碘酸根(IO3-)的形式存在.已知在酸性条件下,IO3-离子能跟碘离子(I-)发生反应生成碘(I2),碘能使淀粉变色,现提供下列试剂和生活中常见的物质:①碘化钾溶液(溶液中含有I-)②白醋③白糖④白酒⑤淀粉⑥纯碱.欲通过实验证明加碘食盐中存在碘酸根离子,必须选用的试剂和物质是( )
| A. | ①⑤⑥ | B. | ①②③ | C. | ①②⑤ | D. | ②④⑥ |
13.氨气在化学工业中用途广泛.一定条件下,合成氨反应的微观过程如图所示.下列说法正确的是( )
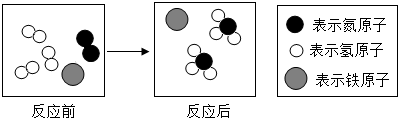

| A. | 该反应属于置换反应 | |
| B. | 参加反应的反应物的微粒数之比为3:1:1 | |
| C. | 该反应中分子总数减少,因此物质的总质量也减少 | |
| D. | 该反应中氢元素化合价升高了,氮元素化合价降低了 |
10.硫酸亚铁铵晶体俗称摩尔盐,化学式为FeSO4•(NH4)2SO4•6H2O,在制药、电镀方面有广泛的应用.某化学兴趣小组的学生用含有少量铜的废铁屑制备硫酸亚铁铵晶体,流程如图:
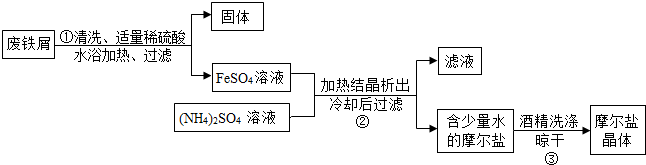
资料:①硫酸亚铁铵晶体易溶于水,不溶于酒精;硫酸亚铁铵晶体在100℃~110℃时分解.
②相关物质的溶解度(单位:g)如下表:
请回答下列问题:
(1)实验前,先用碳酸钠溶液浸泡废铁屑表面油渍.碳酸钠溶液可除去油渍是因为碳酸钠溶液的pH>7(选填“>”、“<”或“=”).
(2)①中发生反应的化学方程式为Fe+H2SO4=FeSO4+H2↑.
(3)操作①中过滤时,要趁热进行的原因是防止过滤时溶液温度降低硫酸亚铁结晶析出,过滤后得到的固体中一定含有的物质是铜(或Cu).
(4)操作③中使用无水酒精洗涤,可快速晾干.这样做的优点是AB(填字母).
A.避免用水洗涤所造成的晶体损耗 B.酒精易挥发,可低温晾干晶体.

资料:①硫酸亚铁铵晶体易溶于水,不溶于酒精;硫酸亚铁铵晶体在100℃~110℃时分解.
②相关物质的溶解度(单位:g)如下表:
| 温度/℃ | FeSO4 | (NH4)2SO4 | FeSO4•(NH4)2SO4•6H2O |
| 10 | 20.0 | 73 | 17.2 |
| 20 | 26.5 | 75.4 | 21.6 |
| 30 | 32.9 | 78 | 28.1 |
(1)实验前,先用碳酸钠溶液浸泡废铁屑表面油渍.碳酸钠溶液可除去油渍是因为碳酸钠溶液的pH>7(选填“>”、“<”或“=”).
(2)①中发生反应的化学方程式为Fe+H2SO4=FeSO4+H2↑.
(3)操作①中过滤时,要趁热进行的原因是防止过滤时溶液温度降低硫酸亚铁结晶析出,过滤后得到的固体中一定含有的物质是铜(或Cu).
(4)操作③中使用无水酒精洗涤,可快速晾干.这样做的优点是AB(填字母).
A.避免用水洗涤所造成的晶体损耗 B.酒精易挥发,可低温晾干晶体.
7.推理是一种重要的化学思维方法,以下推理合理的是( )
| A. | 水和双氧水的组成元素相同,所以它们的化学性质相同 | |
| B. | 离子是带电的原子或原子团,所以带电的粒子一定是离子 | |
| C. | 碱溶液呈碱性,所以呈碱性的溶液都是碱溶液 | |
| D. | 化合物是由不同种元素组成的,所以只含一种元素的物质一定不是化合物 |
11.将下列少量物质分别放入水中,充分搅拌,可以得到无色溶液的是( )
| A. | 高锰酸钾 | B. | 面粉 | C. | 汽油 | D. | 氯化钠 |
12.“单中心铁”可作甲烷高效转化的催化剂,该转化的微观示意图如图,有关转化的说法不正确的是( )
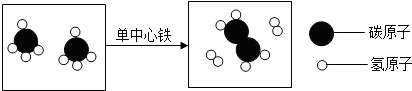

| A. | 反应物和生成物均属于有机物 | |
| B. | “单中心铁”在反应前后质量不变 | |
| C. | “单中心铁”加快了上述反应的速率 | |
| D. | 反应前后原子总数一定没有发生变化 |