题目内容
12.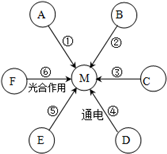 A、B、D均为纯净物,C、E、F均为混合物;①~⑥六条途径(如图)都会产生气体M,实验室可利用途径①、②、③反应来制取M,途径①、②、③、④反应类型相同,途径①反应生成的一种物质N可作为途径②、③反应的催化剂.
A、B、D均为纯净物,C、E、F均为混合物;①~⑥六条途径(如图)都会产生气体M,实验室可利用途径①、②、③反应来制取M,途径①、②、③、④反应类型相同,途径①反应生成的一种物质N可作为途径②、③反应的催化剂.(1)M的化学式为O2.
(2)写出途径④的化学反应式2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,进行此实验时,通常先在D中加入少量氢氧化钠的目的是增强导电性.
(3)常温下,B为白色固体,C为液体,写出途径②反应的化学反应式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(4)工业上需要大量的M时,采用途径⑤,途径⑤是分离液态空气.
分析 根据A、B、D均为纯净物,C、E、F均为混合物,F光合作用会生成气体M,水通电会生成气体M,所以M是氧气,D是水,F是二氧化碳和水,实验室可利用途径①、②、③反应来制取M,途径①、②、③、④反应类型相同,途径①反应生成的一种物质N可作为途径②、③反应的催化剂,所以N是二氧化锰,A是高锰酸钾,B是氯酸钾,C是过氧化氢溶液,然后将推出的物质进行验证即可.
解答 解:(1)A、B、D均为纯净物,C、E、F均为混合物,F光合作用会生成气体M,水通电会生成气体M,所以M是氧气,D是水,F是二氧化碳和水,实验室可利用途径①、②、③反应来制取M,途径①、②、③、④反应类型相同,途径①反应生成的一种物质N可作为途径②、③反应的催化剂,所以N是二氧化锰,A是高锰酸钾,B是氯酸钾,C是过氧化氢溶液,经过验证,推导正确,所以M是O2;
(2)途径④是水在通电的条件下生成氢气和氧气,化学反应式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,进行此实验时,通常先在水中加入少量氢氧化钠的目的是:增强导电性;
(3)常温下,B为白色固体,C为液体,写出途径②是氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,化学反应式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(4)工业上需要大量的氧气时,采用途径⑤,途径⑤是分离液态空气.
故答案为:(1)O2;
(2)2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,增强导电性;
(3)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(4)分离液态空气.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

| A. | 0.9克 | B. | 9克 | C. | 90克 | D. | 1000克 |
| A. | 用澄清石灰水鉴别氧气和二氧化碳 | |
| B. | 用燃着木条鉴别二氧化碳和氮气 | |
| C. | 用硫酸铜溶液鉴别过氧化氢溶液和蒸馏水 | |
| D. | 用肥皂水鉴别硬水和软水 |
| A. | 量筒 | B. | 烧瓶 | C. | 烧杯 | D. | 试管 |
| A. | 矿泉水、氧化镁、空气 | B. | 氮气、过氧化氢、氯酸钾 | ||
| C. | 木炭、水银、牛奶 | D. | 金刚石、冰水、硬水 |
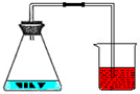 根据如图所示的“铁生锈实验”,回答下列问题.取一块废旧的铁丝,将其剪成几小片,用稀盐酸浸泡片刻.放入锥形瓶中,再向锥形瓶中加入3mL-4mL浓食盐水润湿铁丝,塞紧带导管的单孔塞,导管的另一端塞入红色的水中,几分钟后,观察现象.
根据如图所示的“铁生锈实验”,回答下列问题.取一块废旧的铁丝,将其剪成几小片,用稀盐酸浸泡片刻.放入锥形瓶中,再向锥形瓶中加入3mL-4mL浓食盐水润湿铁丝,塞紧带导管的单孔塞,导管的另一端塞入红色的水中,几分钟后,观察现象. 某元素的原子结构示意图如图,该原子的核电荷数是16,原子核外有3个电子层,最外电子层上有6个电子.在化学反应中,这种原子容易得到电子,变成阴(填阴或阳)离子,其离子符号是S2-.
某元素的原子结构示意图如图,该原子的核电荷数是16,原子核外有3个电子层,最外电子层上有6个电子.在化学反应中,这种原子容易得到电子,变成阴(填阴或阳)离子,其离子符号是S2-.