题目内容
9.由锌、铁、铝、镁四种金属的两种组成混合物,将10g混合物跟足量的稀硫酸反应生成1g氢气,则该混合物中一定含有的金属是( )| A. | 锌 | B. | 铁 | C. | 铝 | D. | 镁 |
分析 可以用极限法和平均值法计算,用极限值计算时,需要分别计算生成1g氢气需要金属的质量,用平均值计算,需要计算混合物的平均相对原子质量.
解答 解:依据化学方程式可知,生成1g,需要锌32.5g,铁28g,镁12g,铝9g,结合平均值思想,混合物中的两种金属需要量分别小于和大于10g,而小于10g的金属只有铝,所以混合物中一定含有铝.
故选:C.
点评 不同考查混合物的计算,题目难度不大,注意平均值法的使用.

练习册系列答案
相关题目
4.在一密闭容器内有四种物质在一定条件下充分反应,测得反应前后各物质的质量如下:
(1)反应后D的质量X为9;
(2)参加反应的物质是A和D.反应生成的物质质量比是1:7.
| 物质 | A | B | C | D |
| 反应前质量/g | 4 | 10 | 1 | 21 |
| 反应后质量/g | 0 | 12 | 15 | X |
(2)参加反应的物质是A和D.反应生成的物质质量比是1:7.
14.下列有关叙述正确的是( )
| A. | 制纯碱需要的原料是食盐和石灰石(或CO2) | |
| B. | 海水晒得的粗盐可以直接吸氨制成氨盐水 | |
| C. | 向氨盐水中通入二氧化碳可得到纯碱,溶液经结晶后得到纯碱固体 | |
| D. | 因为氯化钠水溶液呈中性.所以氨盐水也呈中性 |
6.下列各组物质在水溶液中能大量共存,而且加入无色酚酞溶液后显红色的是( )
| A. | NaOH NaC1 CuSO4 HC1 | B. | KNO3 Na2SO4 NaOH KC1 | ||
| C. | KC1 Ba(NO3)2 HC1 CaC12 | D. | Na2CO3 Ba(OH)2 KNO3 Na2SO4 |
4.下列对分子、原子、离子的认识正确的是( )
| A. | 温度越高,分子运动速率越快 | |
| B. | 原子是最小的粒子,不可再分 | |
| C. | 离子不能直接构成物质 | |
| D. | 固体难压缩,说明固体分子间无间隔 |
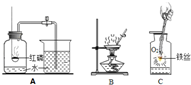 如图所示的是初中化学中的一些重要实验.请回答下列问题:
如图所示的是初中化学中的一些重要实验.请回答下列问题: