题目内容
20.同学们在实验室用混合两种固体药品的办法自制“钾、氮复合肥”,使用到的药品有KCl,K2SO4,NH4HCO3,NH4Cl.同学们制得了成分不同的“钾、氮复合肥”,从中抽取一份作为样品探究其成分,请回答有关问题:限选试剂:稀盐酸,稀硫酸,BaCl2溶液,AgNO3溶液,蒸馏水(1)提出合理假设.所抽样品的成分共有4种可能:
假设1:KCl和NH4HCO3;
假设2:KCl和NH4Cl;
假设3:K2SO4和NH4HCO3;
假设4:K2SO4和NH4Cl.
(2)形成设计思路.
①甲同学提出先用AgNO3溶液确定是否含有KCl,你是否同意?其理由是什么?不同意,因为氯化铵和硝酸银反应也能够生成白色沉淀氯化银.
②乙同学提出先确定是否含有NH4HCO3,则可以选择的试剂是稀盐酸或稀硫酸.
(3)【完成实验方案】请填写实验操作及与表中结论相符的预期现象.
| 实验操作 | 预期现象 | 结论 |
| 步骤1:取少量固体于试管中,滴加适量的稀盐酸或稀硫酸 | 不产生气泡 | 假设2成立 |
| 步骤2:另取少量固体于另一支试管中,加足量的水溶解,滴加适量的氯化钡溶液 | 不产生白色沉淀 |
分析 (1)所抽样品的成分可能是KCl和 NH4HCO3,或KCl和NH4Cl,或K2SO4和 NH4HCO3,或K2SO4和NH4Cl;
(2)氯化钾、氯化铵都能够和硝酸银反应生成氯化银沉淀;
碳酸氢铵能和稀盐酸反应生成氯化铵、水和二氧化碳,能和稀硫酸反应生成硫酸铵、水和二氧化碳;
(3)氯化钾、氯化铵都不能和稀盐酸、稀硫酸、氯化钡反应;
碳酸氢铵能和稀盐酸、稀硫酸反应生成二氧化碳,硫酸钾能和氯化钡反应生成硫酸钡沉淀.
解答 解:(1)所抽样品的成分有4种可能是KCl和 NH4HCO3,也可能是KCl和NH4Cl,也可能是K2SO4和 NH4HCO3,也可能是K2SO4和NH4Cl;
(2)①不能先用AgNO3溶液确定是否含有KCl,这是因为氯化铵和硝酸银反应也能够生成白色沉淀氯化银;
②如果要先确定是否含有NH4HCO3,则可以选择的试剂是稀盐酸或稀硫酸,因为碳酸氢铵能和稀盐酸反应生成氯化铵、水和二氧化碳,能和稀硫酸反应生成硫酸铵、水和二氧化碳;
(3)实验操作1:取少量固体于试管中,滴加适量的稀盐酸或稀硫酸,不产生气泡,说明固体中不含有碳酸氢铵;
实验操作2:另取少量固体于另一支试管中,加足量的水溶解,滴加适量的氯化钡溶液,不产生沉淀,说明固体中不含有硫酸钾;
实验结论:假设2成立.
故答案为:(1)K2SO4和NH4Cl;
(2)①不同意,因为氯化铵和硝酸银反应也能够生成白色沉淀氯化银;②稀盐酸或稀硫酸;
(3)步骤Ⅰ:取少量固体于试管中,滴加适量的稀盐酸或稀硫酸;不产生气泡;
步骤Ⅱ:另取少量固体于另一支试管中,加足量的水溶解,滴加适量的氯化钡溶液;不产生白色沉淀.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案【提出问题】“管道通”中的物质是什么?
【查阅资料】
(1)下水管里的淤积物主要为油污、食物残渣、毛发等.
(2)氢氧化钠是强碱,能去除油污,腐蚀毛发一类的东西.常用于疏通管道.
(3)铝粉呈银灰色.铝与酸、强碱溶液都能反应放出氢气,同时放出大量热.
①铝与盐酸反应的化学方程式是2Al+6HCl═2AlCl3+3H2↑.
②铝与氢氧化钠溶液反应的化学方程式是2Al+2NaOH+2H2O═2NaAlO2+3H2↑
【猜想与验证】打开一盒管道通,内有一袋白色固体颗粒和一袋银灰色粉末.
(1)猜想:白色固体颗粒为氢氧化钠.
| 实验操作 | 实验现象 |
| ①将几粒白色颗粒放在玻璃片上,放置一会儿. | 白色颗粒潮解 |
| ②将几粒白色颗粒放入盛有少量水的试管中,并用手触摸试管外壁. | 试管外壁发烫 |
| ③向步骤②得到的溶液中放入一段羊毛线,加热一段时间. | 羊毛线逐渐消失 |
(2)猜想:银灰色粉末为铝粉.
实验:取该粉末分别置于两支洁净的试管中,向一只试管中滴加稀盐酸,另一只中滴加氢氧化钠溶液,都产生大量气泡且试管外壁温度明显升高,点燃反应产生的气体火焰均呈淡蓝色.
结论:银灰色粉末为铝粉.
【应用】使用“管道通”时,先将银灰色粉状固体添加入被堵塞的管道中,再加入白色固体颗粒,倒入一杯水,堵上管道口.管道内可能出现的现象是ABCD.
A.管道内温度明显升高 B.产生大量气体
C.反应放出大量热 D.气体燃烧后,火焰成淡蓝色.
| A. | 过量摄入油脂会使人发胖,应禁止食用油脂 | |
| B. | 海鲜产品从沿海运到衡阳过程中可以喷洒甲醛溶液防腐 | |
| C. | 在煲好的鸡汤中放入适量的加碘食盐 | |
| D. | 为了保持香肠肉质鲜美,添加过量的亚硝酸钠 |
| A. | +1 | B. | +3 | C. | +7 | D. | +5 |
 如图所示是甲、乙两种固体物质的溶解度曲线.下列说法中正确的是( )
如图所示是甲、乙两种固体物质的溶解度曲线.下列说法中正确的是( )| A. | 甲物质的溶解度大于乙物质的溶解度 | |
| B. | t2℃时,向甲的饱和溶液中加入少量水,甲的溶解度变小 | |
| C. | 乙物质的饱和溶液从t2℃降到t1℃时,溶液中溶质的质量分数保持不变 | |
| D. | t2℃时,甲、乙两物质各50g,分别充分溶解于100g水中,得到的溶液质量分数相同 |
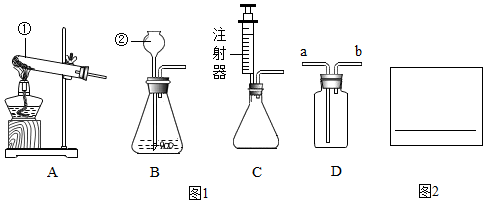
 化学就在我们身边,化学与生活息息相关.
化学就在我们身边,化学与生活息息相关.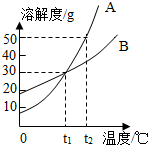 如图是A、B的溶解度曲线.某同学要配制甲、乙两种物质的饱和溶液,而且溶质的质量分数相同,他应该将温度控制在t1℃;把t2℃时150gA的饱和溶液稀释为20%,需加水100 g.
如图是A、B的溶解度曲线.某同学要配制甲、乙两种物质的饱和溶液,而且溶质的质量分数相同,他应该将温度控制在t1℃;把t2℃时150gA的饱和溶液稀释为20%,需加水100 g.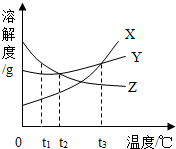 如图是X、Y、Z三种固体物质的溶解度曲线图,根据曲线图回答下列问题.
如图是X、Y、Z三种固体物质的溶解度曲线图,根据曲线图回答下列问题.