题目内容
13.实验室有一瓶存放很久的氢氧化钠,李明同学认为可能变质了,到底是全部变质还是部分变质,同学们进行了探究.请你和他们一起完成以下实验探究.同学们的猜想有:猜想1:全部变质为碳酸钠;
猜想2:部分变质,既有氢氧化钠又有碳酸钠;
猜想3:没有变质,还是氢氧化钠.
李明小组的实验和推断:
| 实验步骤 | 实验现象 | 结论或解释 |
| 1取少量样品于试管中,加入 少量稀盐酸或稀硫酸. | 有气泡产生 | 化学方程式Na2CO3+2HCl═2NaCl+H2O+CO2↑或Na2CO3+H2SO4═Na2SO4+H2O+CO2↑ 猜想3不成立 |
| 2取少量样品于试管中,加水形成溶液,再加入足量的氢氧化钙溶液.再取上层清液,加入酚酞溶液. | 产生白色沉淀 溶液呈现红色 | 猜想2成立 |
分析 根据已有的知识进行分析解答,碳酸钠能与酸反应生成气体,酚酞试液在碱性溶液中变红,要证明氢氧化钠和碳酸钠同时存在,需要加入试剂除去碳酸钠,再加入酚酞试液,据此解答.
解答 解:(1)要证明氢氧化钠是否变质,关键是证明碳酸钠的存在,碳酸钠能与酸反应生成气体,故可以加入稀盐酸或是稀硫酸,有气泡产生,说明猜想3不成立;要证明氢氧化钠的变质程度,关键是证明氢氧化钠的存在,需要加入氯化钙溶液除去碳酸钠,再加入酚酞试液,根据变红证明氢氧化钠的存在,从而证明氢氧化钠是部分变质,故填:
| 实验步骤 | 实验现象 | 结论或解释 |
| 1取少量样品于试管中,加入 少量 稀盐酸或稀硫酸. | 有气泡产生 | 化学方程式 Na2CO3+2HCl═2NaCl+H2O+CO2↑或Na2CO3+H2SO4═Na2SO4+H2O+CO2↑ 猜想3不成立 |
| 2取少量样品于试管中,加水形成溶液,再加入足量的氢氧化钙溶液.再取上层清液,加入 酚酞溶液. | 产生白色沉淀 溶液呈现红色 | 猜想2成立 |
点评 熟练掌握氢氧化钠、碳酸钠的化学性质,知道氢氧化钠的变质的原因并能够选择合适的方法进行检验.记住化学方程式:Na2CO3+2HCl═2NaCl+H2O+CO2↑.

练习册系列答案
相关题目
3.区别下列各组物质,选用的方法或试剂错误的是( )
| A. | 只用酚酞溶液区别盐酸、石灰水和食盐水 | |
| B. | 用熟石灰区别硫酸钾和氯化铵 | |
| C. | 用燃烧的方法区别棉纤维和羊毛纤维 | |
| D. | 用水区别消石灰和苛性钠 |
4.下列事实的结论或解释中不正确的是( )
| A. | 铝制品有抗腐蚀性能--实质是表面生成了致密氧化膜起保护作用 | |
| B. | 公园的桂花开放时满园飘香--说明分子在不断运动 | |
| C. | 酸碱中和反应都能生成水-一实质是H+与OH--结合生成了H2O | |
| D. | 化肥硫酸铵不能和熟石灰混放或混用--硫酸铵和熟石灰发生中和反应 |
1.下列实验操作正确的是( )
| A. | 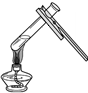 加热液体 | B. | 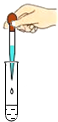 用滴管滴液 | C. | 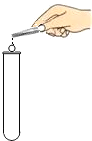 向试管中加固体 | D. |  熄灭酒精灯 |
18.下列关于二氧化碳的说法,错误的是( )
| A. | 干冰用于人工降雨 | B. | 用燃着木条检验二氧化碳 | ||
| C. | 二氧化碳用于灭火 | D. | 用二氧化碳生产碳酸型饮料 |
10.下列对化学知识的整理中正确的一组是( )
| A.化学中常见的“三” | B.化学与安全 |
| 煤、石油、天然气-----三大化石燃料 合金、合成纤维、合成橡胶------三大合成材料 | 煤气泄漏-----关闭气阀、严禁烟火 保鲜水产品-----用甲醛水溶液浸泡 |
| C.化学与健康 | D.常见食物鉴别 |
| 人体缺乏维生素C-----引起夜盲症 人体缺铁-----引发缺铁性贫血 | 硬水和软水-----加肥皂水搅拌 棉花和羊毛-----灼烧,闻气味 |
| A. | 化学中常见的“三” | B. | 化学与安全 | ||
| C. | 化学与健康 | D. | 常见食物鉴别 |
