题目内容
18.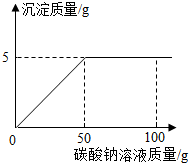 在氯化钙和氯化钠的混合物中加入一定量的水,全部溶解得到50克混合溶液,向该溶液中逐滴加入一定溶质质量分数的碳酸钠溶液,生成沉淀与加入碳酸钠溶液的质量关系如图所示.计算:
在氯化钙和氯化钠的混合物中加入一定量的水,全部溶解得到50克混合溶液,向该溶液中逐滴加入一定溶质质量分数的碳酸钠溶液,生成沉淀与加入碳酸钠溶液的质量关系如图所示.计算:(1)所加碳酸钠溶液的溶质质量分数.
(2)若恰好完全反应时所得溶液的溶质质量分数为10%,则原固体混合物的质量是多少?
分析 (1)根据沉淀的质量和方程式计算碳酸钠和氯化钠的质量,进一步计算碳酸钠溶液的溶质质量分数.
(2)根据恰好完全反应时溶液中溶质的质量分数公式分析.
解答 解:(1)由图象可知,CaCO3的质量为5g,
设原混合物中碳酸钠的质量为x,生成氯化钠的质量为y,参加反应的氯化钙的质量为z.
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 111 100 117
x z 5g y
$\frac{106}{x}$=$\frac{100}{5g}$=$\frac{117}{y}$=$\frac{111}{z}$
x=5.3g,y=5.85g,z=5.55g
所加碳酸钠溶液的溶质质量分数为$\frac{5.3g}{50g}$×100%=10.6%
(3)原固体混合物的质量是w
所以$\frac{5.85g+(w-5.55g)}{50g+50g-5g}$×100%=10%
w=9.2g
答:(1)所加碳酸钠溶液的溶质质量分数为10.6%;
(2)原固体混合物的质量是9.2g.
点评 本题主要考查学生对完全反应的认识,以及应用公式和化学方程式进行正确计算的能力,学生必须有牢固的知识,再加上认真细心的态度,方可完成.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
13.质量为50g溶质质量分数为20%的氢氧化钾溶液和质量为50g溶质质量分数为20%的稀硫酸混合,所得溶液的PH( )
| A. | 小于7 | B. | 等于7 | C. | 大于7 | D. | 不确定 |
12.下列化肥中,属于复合肥的是( )
| A. | K2S04 | B. | NH4HC03 | C. | Ca3(PO4)2 | D. | (NH4)2HPO4 |
9.下列物质的分类正确的是( )
| A. | 混合物:空气、天然气、水蒸气 | B. | 能置换出酸中氢的金属:铝、铁、汞 | ||
| C. | 氧化物:水、酒精、干冰 | D. | 磷单质:红磷、白磷 |

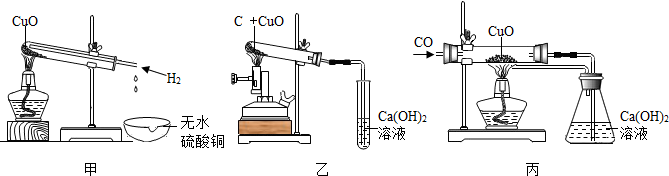
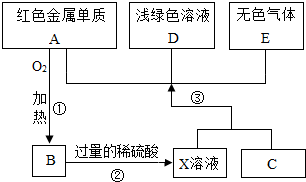 A、B、C、D、E为初中化学常见的物质,其中A、C为金属单质,E为非金属单质,如图所示是它们之间的相互转化关系,则C的化学式为Fe;反应①的基本反应类型是化合反应;E和B在加热条件下反应的化学方程式:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O..
A、B、C、D、E为初中化学常见的物质,其中A、C为金属单质,E为非金属单质,如图所示是它们之间的相互转化关系,则C的化学式为Fe;反应①的基本反应类型是化合反应;E和B在加热条件下反应的化学方程式:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O..