题目内容
14. 实验室常用稀盐酸和石灰石反应制取二氧化碳.
实验室常用稀盐酸和石灰石反应制取二氧化碳.(1)该反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O.
(2)检验生成的气体是二氧化碳的方法是将产生的气体通入澄清的石灰水中,若澄清的石灰水变浑浊,证明生成的气体是二氧化碳.
(3)实验室通常不选用稀硫酸和石灰石反应制取二氧化碳,因生成的微溶物硫酸钙会阻碍反应的进一步进行.某小组经研究,用如图所示方法成功制得了大量CO2(反应物为稀硫酸和石灰石).
①该方法中加热仪器名称是酒精灯;
②推测:在硫酸溶液中加入氯化铵和对溶液加热,目的都是增大硫酸钙在溶液中的溶解能力.
③思考图中方法,你认为相比用稀盐酸和石灰石反应,其改进的出发点是原物质中的盐酸具有挥发性,会进入二氧化碳气体中,对比两种方法,你认为要进行实验改进,关键是干扰实验,所以要进行改进.
分析 (1)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
(2)根据二氧化碳的检验方法进行分析解答.
(3)该方法中加热仪器名称是酒精灯,在硫酸溶液中加入氯化铵和对溶液加热,目的都是增大硫酸钙在溶液中的溶解能力;改进的出发点是:原物质中的盐酸具有挥发性,会进入二氧化碳气体中;干扰实验,所以要进行改进.
解答 解:(1)实验室制取二氧化碳常用稀盐酸和石灰石反应,生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O.故答案为:CaCO3+2HCl=CaCl2+CO2↑+H2O;
(2)检验生成的气体是二氧化碳的方法是将产生的气体通入澄清的石灰水中,若澄清的石灰水变浑浊,证明生成的气体是二氧化碳.故填:将产生的气体通入澄清的石灰水中,若澄清的石灰水变浑浊,证明生成的气体是二氧化碳;
(3)该方法中加热仪器名称是酒精灯,因为硫酸钙微溶于水,会阻碍反应的进行,在硫酸溶液中加入氯化铵,生成的硫酸钙会溶解到氯化铵溶液中,硫酸与碳酸钙的反应就会一直进行下去,目的是增大硫酸钙在溶液中的溶解能力;改进的出发点是:原物质中的盐酸具有挥发性,会进入二氧化碳气体中;干扰实验,所以要进行改进.故答案为:①酒精灯;②增大硫酸钙在溶液中的溶解能力;③原物质中的盐酸具有挥发性,会进入二氧化碳气体中;干扰实验,所以要进行改进.
点评 本考点主要考查了二氧化碳的制取、检验和装置的改进,同时也考查了符号表达式的书写等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案
相关题目
4.一种液体是否是溶液,最充分的条件是( )
| A. | 一种物质均匀地分散到另一种物质中 | |
| B. | 液体均一、稳定 | |
| C. | 溶质被分散成分子或离子的混合物 | |
| D. | 长期静置后液体不分层或无沉淀 |
5.某药品的说明书上标明:本品每克含碘150mg,镁65mg,锌15mg,这里的碘、镁、锌是指( )
| A. | 原子 | B. | 分子 | C. | 元素 | D. | 离子 |
2.下列有关化合价的说法中错误的是( )
| A. | 在化合物中,有显正价的元素,也必有显负价的元素 | |
| B. | 在化合物中,金属元素显正价 | |
| C. | 同种元素在不同化合物中的化合价一定相同 | |
| D. | 离子所带电荷数与对应元素(或原子团)的化合价在数值上相等 |
9.
(1)上表元素中,在地壳内含量最多的金属元素符号是Al;在人体内含量最多的元素符号是O;水中含有的+1价的元素符号是H;
(2)氯化钙的化学式为CaCl2;Na2SO3中S元素的化合价为+4.
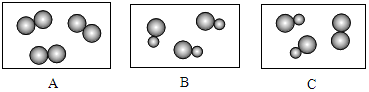
(3)如图表示气体分子示意模型,其中属于化合物的是B(填字母序号),属于混合物的是C(填字母序号).选用上面几种元素,表示A图中的分子,其化学式可能为H2或O2(写出两种即可).
| 元素名称 | 钠 | 钙 | 铝 | 氢 | 氯 | 氧 | 硫 |
(2)氯化钙的化学式为CaCl2;Na2SO3中S元素的化合价为+4.
(3)如图表示气体分子示意模型,其中属于化合物的是B(填字母序号),属于混合物的是C(填字母序号).选用上面几种元素,表示A图中的分子,其化学式可能为H2或O2(写出两种即可).

4.如图5是“XX牌贴身暖宝宝”使用说明书,小王等同学阅读了使用说明后,对它的成分和发热原理产生了兴趣,和同学们一起进行了实验探究.

(1)袋内物质中含有的金属元素至少有2种,其外袋材料属于合成(填“无机非金属”、“合成”或“复合”)材料.
(2)【初步探究成分及发热原理】
【提出问题】:“暖宝宝”为什么能发热?
【做出猜想】:“暖宝宝”发出的热量主要来自铁粉氧化(即生锈)的过程.
【设计实验】:
【继续探究】:小王和同学们想继续探究“暖宝宝”发热后,剩余物质中是否还含有活性炭,他们取适量A袋内物质于烧杯内,加入过量,充分反应后过滤,洗涤、烘干滤渣.为进一步验证黑色滤渣的成分,小王和小李同学分别设计了1、2两个如图所示的装置,点燃滤渣,用澄清石灰水验证产物,你认为图的装置结论更可靠,理由是.同学们分析铁生锈是一个缓慢氧化的过程,“暖宝宝”放热现象之所以很明显是因为:吸附
①铁呈粉末状,活性炭有性,使铁能与氧气、水等接触充分;
②氯化钠能加快铁生锈;
(3)【测定“暖宝宝”中的含铁量】
取一片包装完好的“暖宝宝”,剪开包装,利用袋内物质立即进行实验.
【实验方法】:取样品m g,利用如图3所示装置与药品,测反应后生成气体的体积.
【实验步骤】:
①连接仪器,检查装置气密性;
②将实验所用药品装入各仪器中,记录量气管(水准管中水不会溢出)初始刻度;
③打开分液漏斗活塞,加入足量稀硫酸至不再有气泡冒出.在实验过程中,若烧瓶和量气管内气体压强过大,可将水准管下移(填“上提”或“下移”).
④等恢复至室温,并调节量气管与水准管两边液面相平后,再次记录量气管刻度;
【数据处理】:
若实验条件下,氢气的密度为d g/mL,测得氢气体积为v mL.则该“暖宝宝”中铁粉的质量分数的表达式为$\frac{28dv}{m}$.
【交流讨论】:
利用3装置,即使操作无失误,测量结果仍会偏大,原因是滴入烧瓶内的稀硫酸占一定体积,小王重新设计了一个如图4的实验装置,利用该装置实验时,在气密性良好的前提下,如果往锥形瓶中注入的稀硫酸体积为V1mL,充分反应后,右侧针筒中气体的读数为V2 mL,则反应生成的氢气的体积为V2-V1mL.
(4)【测定“暖宝宝”中的铁、碳质量比】
小李取了一片外袋已有部分破损的“暖宝宝”,剪开包装,利用袋内物质立即进行实验.
【查阅资料】:
①2Fe(OH)3═$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2O
②Fe+2FeCl3═3FeCl2
③在HCl和FeCl3的混合溶液中Fe先与FeCl3反应
【实验记录】:(如图6)
【实验结论】:经该实验测定,新产品的配料中碳粉和铁粉的质量比为1.9:7.28(或95:364),该片已有破损的“暖宝宝”中的剩余铁单质的质量为6.16g.

(1)袋内物质中含有的金属元素至少有2种,其外袋材料属于合成(填“无机非金属”、“合成”或“复合”)材料.
(2)【初步探究成分及发热原理】
【提出问题】:“暖宝宝”为什么能发热?
【做出猜想】:“暖宝宝”发出的热量主要来自铁粉氧化(即生锈)的过程.
【设计实验】:
| 实验操作 | 实验现象 | 解释或结论 | |
| 步骤1 | 取A、B两袋“暖宝宝”,将A袋按使用说明打开外袋取出内袋;而B袋不打开外袋.并将两袋样品放置在同样的环境中. | A袋的“暖宝宝”温度很快上升;B袋温度. | “暖宝宝”发热是由于袋内物质与O2(或空气)接触. |
| 步骤2 | 24小时后,分别剪开A、B两袋,各取少量袋内物质于两支试管中,分别加入适量稀盐酸. | A袋内物质部分溶解,产生黄色溶液;B袋内物质. | 用化学方程式表示产生黄色溶液的反应:Fe2O3+6HCl=2FeCl3+3H2O |
| 【得出结论】:“暖宝宝”发出的热量主要来自铁粉发生氧化(生锈)的过程. | |||
①铁呈粉末状,活性炭有性,使铁能与氧气、水等接触充分;
②氯化钠能加快铁生锈;
(3)【测定“暖宝宝”中的含铁量】
取一片包装完好的“暖宝宝”,剪开包装,利用袋内物质立即进行实验.
【实验方法】:取样品m g,利用如图3所示装置与药品,测反应后生成气体的体积.
【实验步骤】:
①连接仪器,检查装置气密性;
②将实验所用药品装入各仪器中,记录量气管(水准管中水不会溢出)初始刻度;
③打开分液漏斗活塞,加入足量稀硫酸至不再有气泡冒出.在实验过程中,若烧瓶和量气管内气体压强过大,可将水准管下移(填“上提”或“下移”).
④等恢复至室温,并调节量气管与水准管两边液面相平后,再次记录量气管刻度;
【数据处理】:
若实验条件下,氢气的密度为d g/mL,测得氢气体积为v mL.则该“暖宝宝”中铁粉的质量分数的表达式为$\frac{28dv}{m}$.
【交流讨论】:
利用3装置,即使操作无失误,测量结果仍会偏大,原因是滴入烧瓶内的稀硫酸占一定体积,小王重新设计了一个如图4的实验装置,利用该装置实验时,在气密性良好的前提下,如果往锥形瓶中注入的稀硫酸体积为V1mL,充分反应后,右侧针筒中气体的读数为V2 mL,则反应生成的氢气的体积为V2-V1mL.
(4)【测定“暖宝宝”中的铁、碳质量比】
小李取了一片外袋已有部分破损的“暖宝宝”,剪开包装,利用袋内物质立即进行实验.
【查阅资料】:
①2Fe(OH)3═$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2O
②Fe+2FeCl3═3FeCl2
③在HCl和FeCl3的混合溶液中Fe先与FeCl3反应
【实验记录】:(如图6)
【实验结论】:经该实验测定,新产品的配料中碳粉和铁粉的质量比为1.9:7.28(或95:364),该片已有破损的“暖宝宝”中的剩余铁单质的质量为6.16g.
 如图是给病人输液用的氯化钠注射液的标签,请根据该标签提供的信息回答:要配制1000mL这种注射溶液(密度为1g/cm3),需氯化钠多少克?
如图是给病人输液用的氯化钠注射液的标签,请根据该标签提供的信息回答:要配制1000mL这种注射溶液(密度为1g/cm3),需氯化钠多少克?