题目内容
9.取一定量的氧化铁和氧化亚铁的混合物,加入200g9.8%的稀硫酸,恰好完全反应生成盐和水.则原固体混合物中氧元素的质量是( )| A. | 9.8g | B. | 3.6g | C. | 3.2g | D. | 19.6g |
分析 根据氧化铁和氧化亚铁与稀硫酸反应的化学方程式结合硫酸的质量,根据氧元素的质量守恒分析解答.
解答 解:氧化铁和氧化亚铁与稀硫酸反应的化学方程式为:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;FeO+H2SO4═FeSO4+H2O;由于氧化亚铁和氧化铁的混合物与200克、9.8%的稀硫酸恰好完全反应,分析化学方程式可知氧化物中氧元素全部转变为水中的氧元素,计算出水的质量进而计算出所含氧元素的质量即可;
设生成水的质量是x:由方程式可以看出硫酸与生成水的关系为
H2SO4 ~H2O~~~O
98 16
200g×9.8% x
$\frac{98}{16}=\frac{200g×9.8%}{x}$
x=3.2g
故选C
点评 本题很好的考查了质量守恒定律的应用,解答时首先分析实验的反应原理,再根据反应原理,根据化学方程式计算出该样品中某一成分的质量,得出所要探究的物质中该成分的含量.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.某化学兴趣小组对一包完全变质的生石灰干燥剂产生了好奇,为确定其成分展开如下探究:
[提出问题]这包已完全变质的干燥剂成分是什么?
[猜想]猜想I:Ca(OH)2
猜想 II:Ca(OH)2 和 CaCO3
猜想 III:CaCO3
[实验探究]
(1)取少量样品于试管中,向其中滴加少量稀盐酸,无气泡产生.于是小莉认为没有CaCO3,小晶却不同意小莉的结论,理由是加入盐酸的量不足.
(2)为进一步确定其成分,小组同学共同设计了如下方案,请你完成实验报告.
[实验反思](1)步骤②中有关反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H2O;CaCO3+2HCl=CaCl2+H2O+CO2↑.
(2)生石灰变质过程可简述为:生石灰吸收H2O变成熟石灰,熟石灰吸收CO2变成碳酸钙.
[提出问题]这包已完全变质的干燥剂成分是什么?
[猜想]猜想I:Ca(OH)2
猜想 II:Ca(OH)2 和 CaCO3
猜想 III:CaCO3
[实验探究]
(1)取少量样品于试管中,向其中滴加少量稀盐酸,无气泡产生.于是小莉认为没有CaCO3,小晶却不同意小莉的结论,理由是加入盐酸的量不足.
(2)为进一步确定其成分,小组同学共同设计了如下方案,请你完成实验报告.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,加适量水溶解,向试管中滴加几滴酚酞溶液. | 溶液变成红色 | 猜想II成立 |
| ②另取少量样品于试管中,加适量水溶 解,加 入过量的稀盐酸 | 有气泡产生 |
(2)生石灰变质过程可简述为:生石灰吸收H2O变成熟石灰,熟石灰吸收CO2变成碳酸钙.
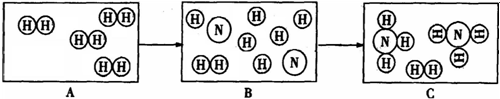
18.下列推断正确的是( )
| A. | 在加压条件下,6000L 氧气可装入容积为 40L 的钢瓶中,由此推断氧气分子变小了 | |
| B. | 蔗糖在热水中的溶解速度更快,由此推断在受热情况下分子运动速率加快 | |
| C. | 中和反应生成盐和水,由此推断生成盐和水的反应一定是中和反应 | |
| D. | 碱能使酚酞试液变红,由此推断能使酚酞试液变红的物质一定是碱 |
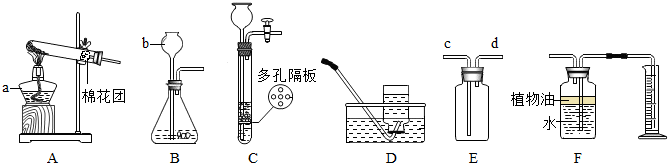 (1)写出下列仪器名称:a酒精灯;b长颈漏斗.
(1)写出下列仪器名称:a酒精灯;b长颈漏斗.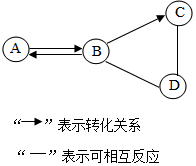 A、B、C、D 为初中化学常见的四种物质,它们之间有如图所示的转化关系(部分物质和反应条件已略去).
A、B、C、D 为初中化学常见的四种物质,它们之间有如图所示的转化关系(部分物质和反应条件已略去).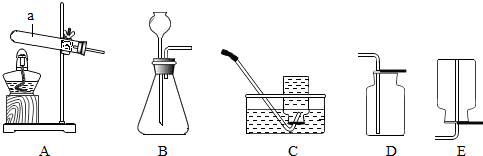
 如图是某工业盐产品质量指标.为了测定该工业盐中氯化钠的质量分数,取100g该工业盐进行实验:①测得水的质量分数为3.36%;②用碳酸钠来测定杂质氯化钡的质量时,得到0.985g沉淀.(碳酸钠与氯化钡反应的化学方程式:
如图是某工业盐产品质量指标.为了测定该工业盐中氯化钠的质量分数,取100g该工业盐进行实验:①测得水的质量分数为3.36%;②用碳酸钠来测定杂质氯化钡的质量时,得到0.985g沉淀.(碳酸钠与氯化钡反应的化学方程式: