题目内容
9.请用所学化学知识解释下列原理(能写化学方程式要写化学方程式).(1)浓硫酸可用作某些气体的干燥剂,说明它们具有吸水性.
(2)能用盐酸除去热水瓶壁上的水垢(碳酸钙)的原理是2HCl+CaCO3=CaCl2+CO2↑+H2O.
(3)氢氧化钠需密封保存,原因是易潮解;2NaOH+CO2=Na2CO3+H2O.
(4)用含Al(OH)3的药物治疗胃酸过多的原理Al(OH)3+3HCl=AlCl3+3H2O.
(5)洗涤剂能除去油污,是因为它具有乳化功能.
(6)在铁制品表面涂油、刷漆或镀铬等都能防止铁生锈,其原理是隔绝氧气(空气)和水.
分析 (1)根据浓硫酸具有吸水性解答;
(2)根据盐酸和碳酸钙反应解答;
(3)根据氢氧化钠固体易吸收水分并且和空气中的二氧化碳反应解答;
(4)根据方程式的写法考虑;
(5)根据乳化作用考虑;
(6)根据生锈的条件考虑.
解答 解:
(1)浓硫酸可用作某些气体的干燥剂,说明它们具有吸水性;
(2)能用盐酸除去热水瓶壁上的水垢(碳酸钙)的原理是2HCl+CaCO3=CaCl2+CO2↑+H2O;
(3)氢氧化钠需密封保存,原因是氢氧化钠固体易吸收水分并且和空气中的二氧化碳反应,反应原理为:2NaOH+CO2=Na2CO3+H2O;
(4)反应物是氢氧化铝和盐酸,生成物是氯化铝和水,用观察法配平即可.反应原理为:Al(OH)3+3HCl=AlCl3+3H2O;
(5)洗涤剂能除去油污是利用乳化原理将大的油滴颗粒分解成小的油滴微粒,便于用水冲掉;
(6)铁生锈的条件是与氧气和水共同作用的结果,所以在铁制品表面涂油、刷漆或镀铬等都能防止铁生锈,原理是既隔绝了空气也隔绝了水分,使铁制品缺少生锈的条件,而不能生锈;
故答案为:
(1)吸水;
(2)2HCl+CaCO3=CaCl2+CO2↑+H2O;
(3)易潮解;2NaOH+CO2=Na2CO3+H2O;
(4)Al(OH)3+3HCl=AlCl3+3H2O;
(5)乳化;
(6)隔绝氧气(空气)和水.
点评 本题考查了化学与生活的知识,完成此题,可以依据题干提供的信息结合已有的知识进行.书写反应的化学方程式要注意配平.

练习册系列答案
相关题目
19.下列除去物质中的少量杂质(括号内为杂质)的方法,正确的是( )
| A. | CO(CO2)--在足量的氧气中燃烧 | |
| B. | MnO2粉末(KCl)--溶解、过滤、洗涤、干燥 | |
| C. | FeSO4溶液(CuSO4)--加入足量锌粉、过滤 | |
| D. | NaCl晶体(Na2CO3)--加入适量稀硫酸蒸发结晶 |
20.如图是初中化学中的一些基本实验,不能达到实验目的是( )
| A. | 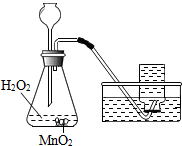 制取氧气 | B. | 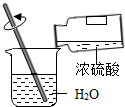 稀释浓硫酸 | ||
| C. | 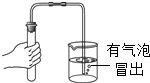 检查装置气密性 | D. | 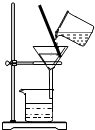 粗盐过滤 |
18.形成化学观念是化学学习的任务之一,下列说法中错误的是( )
| A. | 分子、原子、离子都是构成物质的微粒 | |
| B. | 化学变化的过程实质上是原子重新组合的过程 | |
| C. | 物质在水中的溶解过程实质上是原子重新组合的过程 | |
| D. | 水的三态变化中,分子的能量、运动速率改变 |
19.下列防锈措施不正确的是( )
| A. | 铁制品表面镀锌 | B. | 洗净铁制品表面的油膜 | ||
| C. | 制成合金后使用 | D. | 保持铁制品表面清洁干燥 |