题目内容
12. 如图是a、b、c三种物质的溶解度曲线.根据图回答:
如图是a、b、c三种物质的溶解度曲线.根据图回答:(1)t1℃时,a和c的溶解度相等.
(2)t3℃时,把30克 a、b、c三种物质分别加入到盛有100克水的烧杯中不断搅拌,所得溶液的溶质质量分数大小关系C(填字母);
A.a>b>c B.b>a=c
C.a=b>c D.b>a>c
(3)在t2℃下,将c物质的不饱和溶液变为饱和溶液,下列有关说法不正确的是D(填字母).
A.溶剂的质量可能变小 B.溶液的质量可能变大
C.溶质的质量分数一定变大 D.溶质的质量一定不变
(4)t1℃时,从含有a、c两种溶质的饱和溶液中分离出c的办法是:升温结晶.
分析 (1)溶解度曲线的交点表示该温度下两物质的溶解度相等;
(2)根据t3℃时abc的溶解度考虑;
(3)根据C物质的不饱和溶液变为饱和溶液的方法进行分析;
(4)根据ac的溶解度随温度变化情况分析.
解答 解:
(1)t1℃时,a和c的溶解度曲线交于一点,二者的溶解度相等;
(2)在t3℃时a物质的溶解度为50g,b物质的溶解度等于38g,丙的溶解度小于20g,所以将30ga、b、c分加入到盛有100g水的烧杯中,ab均能全部溶解,c能溶解的质量小于20g,所以在t3℃时所得溶液的溶质质量分数大小关系是a=b>c;
(3)C物质的溶解度随温度升高而减小,所以不饱和溶液变为饱和溶液的方法有:加入溶质、蒸发溶剂、升温;
因为温度不变,不能采取升温的方法;
A、若采取蒸发溶剂的方法,则溶剂减小,若采取加入溶质、升温的方法,溶剂的质量不变,所以溶剂的质量可能变小,正确;
B、若采取加入溶质的方法,则溶质的质量增加,溶剂的质量不变,则溶液质量变大,若采取升温的方法,溶液的质量不变,采取蒸发溶剂的方法,溶液的质量减小,所以溶质的质量可能变大,正确;
C、若采取增加溶质的方法,溶质增加,溶质的质量分数增大,若采取蒸发溶剂的方法,溶液中溶剂的质量减小,则溶质的质量分数变大,正确;
D、若采取加入溶质的方法,溶质的质量增加,故错误;
(4)a的溶解度随温度升高而增大,且变化较大,c 的溶解度随温度升高而减小,所以t1℃时,从含有a、c两种溶质的饱和溶液中分离出c,可采取升温结晶的办法;
故答案为:(1)t1℃;(2)C; (3)D;(4)升温结晶.
点评 解答本题关键是要知道溶解度曲线表示的意义,知道溶解度如何比较大小,饱和溶液溶质质量分数的计算,饱和溶液与不饱和溶液的相互转化,知道溶解度的含义.

| A. | 加入过量浓H2SO4微热后,过滤,洗涤 | |
| B. | 加强热或在空气中灼热 | |
| C. | 加适量水,加热,过滤,洗涤 | |
| D. | 加适量稀H2SO4,微热,过滤,洗涤 |
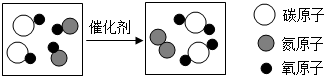
| A. | 该反应方程式为:CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$N2+CO2 | |
| B. | 该反应前后分子的种类没有改变 | |
| C. | 该反应前后原子的数目发生改变 | |
| D. | 该反应体现了一氧化碳的还原性 |
| A. | 碘溶于酒精 | B. | 碳酸钙溶于稀盐酸 | ||
| C. | 高锰酸钾溶于水 | D. | 雪融化成水 |
| A. | 向上排空气法 | B. | 向下排空气法 | C. | 排水法 | D. | 排空气法 |
| A. | NH4H2PO4 | B. | Ca(H2PO4)2+CaSO4 | C. | K2SO4 | D. | NH4HCO3 |
 如图是A、B、C三种物质的溶解度曲线,据图回答:
如图是A、B、C三种物质的溶解度曲线,据图回答: