题目内容
11.某混合物由CaSO3和CaSO4两种化合物组成,试求:(1)该混合物中Ca与S的原子个数比是多少?
(2)该混合物中Ca与S的质量比是多少?
(3)如果上述混合物中氧的质量分数为46%,则Ca的质量分数是多少?
分析 (1)根据物质的结构来分析;
(2)根据化合物中元素的质量比来分析;
(3)根据物质的组成以及化合物中元素的质量分数计算方法来分析.
解答 解:(1)由CaSO3和CaSO4两种物质的化学式可知,两种物质中钙原子与硫原子的个数比均为1:1;故填:1:1;
(2)由CaSO3和CaSO4两种物质的化学式可知,两种物质中钙原子与硫原子的个数比均为1:1,则钙元素与硫元素的质量比为:40:32=5:4;故填:5:4;
(3)混合物中氧的质量分数为46%,则混合物中钙元素与硫元素共占1-46%=54%,其中钙元素的质量分数为:54%×$\frac{5}{9}$=30%,故填:30%.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
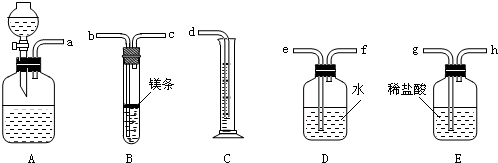
1.下列有关实验及其现象描述不正确的是( )
| A. | 红磷在氧气中燃烧产生大量白烟 | |
| B. | 铁在空气中燃烧火星四射,生成黑色固体 | |
| C. | 电解水与电源负极相连的玻璃管内产生的气体可以燃烧,产生淡蓝色火焰 | |
| D. | 二氧化碳通入紫色的石蕊试液后溶液变成红色 |
19.下列实验现象或结论的描述中错误的是( )
| A. | 碘易溶于水 | |
| B. | 高锰酸钾几乎不溶于汽油 | |
| C. | 乙醇能与水互溶 | |
| D. | 水和植物油混合后用力振荡可形成乳浊液 |
16.在氧气中完全燃烧相同质量的下列物质,消耗氧气最少的是( )
| A. | CO | B. | S | C. | P | D. | C |
1.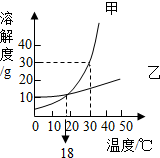 下列对如图所示的溶解度曲线图分析正确的是( )
下列对如图所示的溶解度曲线图分析正确的是( )
 下列对如图所示的溶解度曲线图分析正确的是( )
下列对如图所示的溶解度曲线图分析正确的是( )| A. | 30℃时,甲的溶解度小于乙的溶解度 | |
| B. | 0~30℃时,乙物质溶解度随温度变化比甲大 | |
| C. | 18℃时,甲、乙两物质的溶解度相等 | |
| D. | 甲物质的溶解度大于乙物质的溶解度 |