题目内容
6.某兴趣小组设计实验探究红砖粉对过氧化氢溶液能否起催化作用:实验步骤:①A、B试管中均盛等体积等浓度的过氧化氢溶液;②向A中加入1克红砖粉.分别将带火星的木条放置在A、B试管口,A管口木条复燃,B管口木条不复燃;③反应结束后,将A中混合物过滤、洗涤、烘干得到滤渣;④观察滤渣的颜色和状态;⑤称量滤渣的质量为X克;⑥将滤渣加入到B试管中,伸入带火星木条,木条复燃.
请回答:(1)实验步骤①中设计A、B两试管的目的是对比;分析步骤②的实验现象,得出的结论是红砖粉能加快过氧化氢的分解.
(2)若省略步骤④,能否达到实验目的?能(能或否),你的理由是作为催化剂与颜色和状态改变无关;步骤⑤中X=1g时,能进一步证明红砖粉是催化剂.设计步骤⑥的作用是为了验证红砖粉的化学性质不变.
(3)若要比较红砖粉与二氧化锰的催化效率,需要控制一致的条件包括①②③④(填序号)
①实验温度 ②H2O2的浓度 ③催化剂质量 ④催化剂的颗粒大小.
分析 (1)根据实验步骤①中设计A、B两试管的目的是作对比试验,氧气具有助燃性,能使带火星的木条复燃进行解答;
(2)根据催化剂与颜色和状态改变无关,所以省略步骤④,能达到实验目的进行解答;
(3)根据比较红砖粉与二氧化锰的催化效率,除了催化剂的种类不同外,其它的量都需要相同进行解答.
解答 解:(1)实验步骤①中设计A、B两试管的目的是作对比试验,氧气具有助燃性,能使带火星的木条复燃,所以由步骤②的实验现象,得出的结论是;
(2)催化剂与颜色和状态改变无关,所以省略步骤④,能达到实验目的,催化剂反应前后质量不变,所以步骤⑤中X=1g时,能进一步证明红砖粉是催化剂.设计步骤⑥的作用是为了验证红砖粉的化学性质不变;
(3)根据比较红砖粉与二氧化锰的催化效率,除了催化剂的种类不同外,其它的量都需要相同,所以需要控制一致的条件包括①实验温度、②H2O2的浓度、③催化剂质量、④催化剂的颗粒大小.
故答案为:(1)对比;红砖粉能加快过氧化氢的分解;
(2)能;作为催化剂与颜色和状态改变无关;1g;为了验证红砖粉的化学性质不变;
(3)①②③④.
点评 本题的思路很明确,就是验证红砖粉对过氧化氢分解是否有催化作用,按照探究实验的步骤按部就班的完成.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
16.下列变化中,属于化学变化的是( )
| A. | 浓盐酸挥发 | B. | 冰雪融化 | C. | 食物变质 | D. | 空气液化 |
 用
用 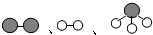 分别表示N2、H2、NH3.在催化剂表面(图中表示催化剂表面)N2和H2反应合成氨的反应过程可用五张图表示如下:
分别表示N2、H2、NH3.在催化剂表面(图中表示催化剂表面)N2和H2反应合成氨的反应过程可用五张图表示如下:
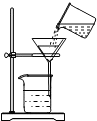 某研究性小组的同学对江津区内某地水质状况进行调查研究,将取得的水样进行过滤,据右图回答下列问题:
某研究性小组的同学对江津区内某地水质状况进行调查研究,将取得的水样进行过滤,据右图回答下列问题: