题目内容
(1)①某化学兴趣小组他们查阅资料后找到了这样一段话:“二氧化硫能使KMnO4溶液褪色(由紫红色变成无色),反应方程式为:5SO2+2KMnO4+2H2O═K2SO4+2MnSO4+2”.然而方程式中最后一种物质的化学式印刷不清楚,根据上下文了解到该物质 是一种酸,请根据已学知识推测其化学式: .反应后生成的MnSO4中Mn元素化合价为 .②盐往往是由离子构成的.如:KMnO4由K+和MnO4-构成,K2SO4由K+和SO42-构成.盐的晶体或溶液的颜色通常是由构成它的离子决定的.
请根据上述查阅到的资料推测:KMnO4溶液呈现的紫红色可能是由 离子表现出来的(填离子符号),理由是
(2)中和4g的氢氧化钠固体需某种稀盐酸的质量为ag,如果将4g的氢氧化钠固体放在空气中一段时间后,再与同样的稀盐酸反应,需该稀盐酸的质量为bg,则a与b的关系是(填“大于”、“小于”、“等于”), 对此总结出一个简单的规律是 .
(3)氧化汞受热时的变化可用下图表示(图中大圆圈表示汞原子,小圆圈表示氧原子)请仿照氧化汞受热变化示意图在左图中画出水通电分解生成氢气和氧气的变化图 (大圆圈表示氧原子,小圆圈表示氢原子)

【答案】分析:(1)①依据质量守恒定律,利用原子在化学反应前后种类与数目均不变,对照反应物及生成物中各原子的种类与个数,最后确定所需判断物质的化学式,然后根据正负化合价代数和为零的原则确定元素的化合价.
②依据反应前后溶液颜色的变化,分析溶液中离子的组成,结合题目信息,最后前后对照,得出结论.
(2)因为反应前后元素的质量不变,可根据钠元素形成的化合物进行分析.
(3)首先确定水分子、氢分子、氧分子的模型,然后按照反应前后分子分解成原子,原子再重新组合成分子画图.
解答:(1)①根据原子在化学反应前后种类与数目均不变可得:未知物的化学式中含义氢、硫、氧三种原子,氢、硫、氧的个数分别为:2、1、4,得其化学式为:H2SO4;反应后生成的MnSO4中硫酸根为-2价,故Mn元素化合价为+2.
故答案为:H2SO4,+2;
②根据反应的化学方程式,反应前溶液中的离子有:K+、MnO4-,反应后溶液中的离子有:K+、SO42-、Mn2+,反应后溶液无色,说明K+、SO42-、Mn2+无色,可得呈现的紫红色是MnO4-,故答案为:MnO4-,反应后无色溶液中存在K+,说明K+无色,故紫红色是由MnO4-表现出来的(合理答案均可得分).
(2)氢氧化钠与盐酸反应生成氯化钠和水,变质后的碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,可见钠元素全部转化为氯化钠,根据元素质量不变,氢氧化钠直接转变成氯化钠的质量和变质后再转化成氯化钠的质量是相同的,那么需要的盐酸的质量就是相同的.
故答案为:等于,等质量的氢氧化钠无论是否变质,与盐酸反应的量是相等的;
(3)一个水分子是由两个氢原子和一个氧原子构成的,一个氢分子是由两个氢原子构成的,一个氧分子是由两个氧原子构成的,由此可画出分解的微观示意图;
故答案为: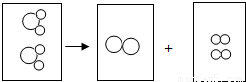
点评:此题属于综合探究题,涉及知识面广,对学生思维能力要求高,既考查知识的识记、理解、迁移、运用,又考查分析、对比、归纳等思维能力,符合素质教育培养学生能力的要求,是中考方向,对这类题目要重点训练.
②依据反应前后溶液颜色的变化,分析溶液中离子的组成,结合题目信息,最后前后对照,得出结论.
(2)因为反应前后元素的质量不变,可根据钠元素形成的化合物进行分析.
(3)首先确定水分子、氢分子、氧分子的模型,然后按照反应前后分子分解成原子,原子再重新组合成分子画图.
解答:(1)①根据原子在化学反应前后种类与数目均不变可得:未知物的化学式中含义氢、硫、氧三种原子,氢、硫、氧的个数分别为:2、1、4,得其化学式为:H2SO4;反应后生成的MnSO4中硫酸根为-2价,故Mn元素化合价为+2.
故答案为:H2SO4,+2;
②根据反应的化学方程式,反应前溶液中的离子有:K+、MnO4-,反应后溶液中的离子有:K+、SO42-、Mn2+,反应后溶液无色,说明K+、SO42-、Mn2+无色,可得呈现的紫红色是MnO4-,故答案为:MnO4-,反应后无色溶液中存在K+,说明K+无色,故紫红色是由MnO4-表现出来的(合理答案均可得分).
(2)氢氧化钠与盐酸反应生成氯化钠和水,变质后的碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,可见钠元素全部转化为氯化钠,根据元素质量不变,氢氧化钠直接转变成氯化钠的质量和变质后再转化成氯化钠的质量是相同的,那么需要的盐酸的质量就是相同的.
故答案为:等于,等质量的氢氧化钠无论是否变质,与盐酸反应的量是相等的;
(3)一个水分子是由两个氢原子和一个氧原子构成的,一个氢分子是由两个氢原子构成的,一个氧分子是由两个氧原子构成的,由此可画出分解的微观示意图;
故答案为:

点评:此题属于综合探究题,涉及知识面广,对学生思维能力要求高,既考查知识的识记、理解、迁移、运用,又考查分析、对比、归纳等思维能力,符合素质教育培养学生能力的要求,是中考方向,对这类题目要重点训练.

练习册系列答案
相关题目


 (2013?信阳一模)某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示)的溶液,他们对此产生了兴趣.
(2013?信阳一模)某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示)的溶液,他们对此产生了兴趣.


