题目内容
16.分类、归纳、分析、推理等是化学学习中常用的思想和方法.下列相关说法不正确的是( )| A. | 分类:生铁、天然气、冰水混合物都属于混合物 | |
| B. | 归纳:酸和碱中和一定都含有氢元素 | |
| C. | 分析:金刚石和石墨物理性质差异很大,是因为碳原子的排列方式不同 | |
| D. | 推理:碱性溶液能使物色酚酞变红,所以能使酚酞变红的溶液pH一定大于7 |
分析 A、根据混合物的定义解答;
B、根据酸、碱的定义进行分析解答;
C、根据金刚石和石墨物理性质差异很大,是因为碳原子的排列方式不同解答;
D、根据碱性溶液能使酚酞试液变红解答;
解答 解:
A、生铁、天然气都是混合物,、冰水混合物石水,属于纯净物,故错误;
B、酸和碱中和一定都含有氢元素,故正确;
D、金刚石和石墨物理性质差异很大,是因为碳原子的排列方式不同,故正确;
D、碱性溶液能使酚酞试液变红,能使酚酞试液变红的溶液一定是碱性溶液,溶液的pH一定大于7,故正确;
答案:A
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
6.小明同学利用一瓶敞口放置已久的NaOH溶液进行了一些实验探究.
[提出问题]这瓶NaOH溶液变质程度如何呢?
[提出猜想]小明的猜想:NaOH溶液部分变质
[实验探究]小明设计了如下实验来验证自己的猜想,请根据表中内容填写实验时的现象.
[实验反思]
(1)下列物质①Ca(OH)2溶液 ②Ba(NO3)2溶液 ③BaCl2溶液,能替代小明实验中CaCl2溶液的是②③
(2)请用化学方程式表示氢氧化钠溶液变质的原因2NaOH+CO2═Na2CO3+H2O
[拓展应用]现向烧杯中加入100g这种已部分变质的NaOH溶液,再滴加溶质质量分数为11.1%的CaCl2溶液100g,产生沉淀质量与所加CaCl2溶液质量的关系如图所示.
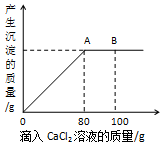
(1)B点处所得溶液中溶质为NaCl和CaCl2 (写化学式)
(2)求反应结束后烧杯中沉淀的质量.
[提出问题]这瓶NaOH溶液变质程度如何呢?
[提出猜想]小明的猜想:NaOH溶液部分变质
[实验探究]小明设计了如下实验来验证自己的猜想,请根据表中内容填写实验时的现象.
| 实验步骤 | 现象 | 结论 |
| 取少量NaOH溶液样品于试管中,先滴加足量CaCl2溶液,然后再滴加酚酞试液 | NaOH部分变质 | |
(1)下列物质①Ca(OH)2溶液 ②Ba(NO3)2溶液 ③BaCl2溶液,能替代小明实验中CaCl2溶液的是②③
(2)请用化学方程式表示氢氧化钠溶液变质的原因2NaOH+CO2═Na2CO3+H2O
[拓展应用]现向烧杯中加入100g这种已部分变质的NaOH溶液,再滴加溶质质量分数为11.1%的CaCl2溶液100g,产生沉淀质量与所加CaCl2溶液质量的关系如图所示.

(1)B点处所得溶液中溶质为NaCl和CaCl2 (写化学式)
(2)求反应结束后烧杯中沉淀的质量.
7.下列图象能正确反映对应的变化关系的是( ) 

| A. | 常温下,向硝酸钾的不饱和溶液中加入硝酸钾晶体 | |
| B. | 将生锈严重的铁钉加入到足量的稀盐酸中 | |
| C. | 向一定质量的稀盐酸溶液中不断加入CaCO3 | |
| D. | 将等质量的镁和锌分别加入到过量、等质量分数的稀盐酸中 |
11.小新同学用20g含碳酸钠53%的天然碱,制取氢氧化钠用于制作“叶脉书签”(杂质不参加反应).操作过程如下:

请计算:(1)20g样品中碳酸钠的质量.
(2)反应后所得滤液中氢氧化钠的质量分数为多少?

请计算:(1)20g样品中碳酸钠的质量.
(2)反应后所得滤液中氢氧化钠的质量分数为多少?
1.建立微观和宏观之间的联系是一种科学的思维方式,下列叙述错误的是( )
| A. | 金刚石和石墨的物理性质差异较大,是因为构成它们的微粒种类不同 | |
| B. | 冰和干冰的化学性质存在差异,因为构成它们的微粒种类不同 | |
| C. | 酸碱中和反应都生成水,其实质是H+与OH-结合生成了H2O | |
| D. | NaOH和KOH都具有碱性,其原因是在水中均能解离出OH- |
8.为了测定乙烯(C2H4)在氧气不足时的燃烧产物,将一定量的乙烯和氧气置于一个密闭容器中引燃,测得反应前后各物质的质量如表:
(1)a值是1.4.
(2)该反应的化学方程式为3C2H4+8O2$\frac{\underline{\;点燃\;}}{\;}$6H2O+4CO2+2CO.
| 物质 | 乙烯 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 2.1 | 6.4 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 2.7 | 4.4 | a |
(2)该反应的化学方程式为3C2H4+8O2$\frac{\underline{\;点燃\;}}{\;}$6H2O+4CO2+2CO.
8.实验操作正确的是( )
| A. |  点燃酒精灯 | B. |  取用粉末状固体 | C. |  取用块状固体 | D. |  加热液体 |
9.下列微粒中能保持氢气化学性质的是( )
| A. | 2H | B. | H2 | C. | H | D. | H+ |
 A、B、C、D为初中化学常见的物质,它们之间存在一定的关系,请根据下列叙述回答问题.“-”表示两端的物质能反应,“→”表示物质间存在转化关系.(部分生成物和反应条件已略去).
A、B、C、D为初中化学常见的物质,它们之间存在一定的关系,请根据下列叙述回答问题.“-”表示两端的物质能反应,“→”表示物质间存在转化关系.(部分生成物和反应条件已略去).