题目内容
12.氢氧化钠固体曝露在空气中一段时间会吸收水而潮解,并吸收二氧化碳而变质,故质量会增大,反应的化学方程式为2NaOH+CO2═Na2CO3+H2O,如想检测氢氧化钠是否变质,可用稀盐酸,现象有气泡产生,反应的化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑.分析 根据氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳进行分析.
解答 解:氢氧化钠固体曝露在空气中一段时间会吸收水而潮解,并吸收二氧化碳而变质,氢氧化钠和二氧化碳反应生成碳酸钠和水,所以质量会增大,化学方程式为:2NaOH+CO2═Na2CO3+H2O,如想检测氢氧化钠是否变质,可用稀盐酸,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,实验现象为:有气泡产生,化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑.
故答案为:(1)水,二氧化碳,增大,2NaOH+CO2═Na2CO3+H2O,稀盐酸,有气泡产生,Na2CO3+2HCl=2NaCl+H2O+CO2↑.
点评 本题主要考查了氢氧化钠的性质,完成此题,可以依据已有的知识结合质量守恒定律的实质完成.

练习册系列答案
相关题目
3.在以下的叙述中,你认为正确的是( )
| A. | “干冰升华”是由于分子本身的体积急剧增大 | |
| B. | 在房间里放一盆水可以防止煤气中毒 | |
| C. | 石墨用做电极,利用了它的物理性质 | |
| D. | 木炭在氧气中燃烧时,产生大量的白烟 |
20.根据酸、碱、盐的溶解性能判断,下列关于物质的溶解性叙述正确的是( )
| A. | 硫酸盐少数溶于水 | B. | 碳酸盐都不溶于水 | ||
| C. | 钠盐都能溶于水 | D. | 碱多数难溶于水 |
7.下列固体物质中加入稀盐酸能鉴别的是( )
| A. | NaCl和NaOH | B. | NaCl和Na2CO3 | C. | Na2CO3和KHCO3 | D. | Na2CO3和CaCO3 |
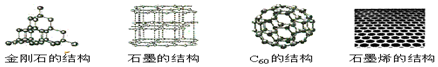
17.石墨烯是新发现的二维空间材料,它是石墨制成的新型碳单质,金刚石、石墨、C60和石墨烯的结构示意图如下所示,下列关于这四种物质的说法中正确的是( )

| A. | 都是黑色固体 | |
| B. | 都质软可作润滑剂 | |
| C. | 碳原子排列方式不同 | |
| D. | 在氧气中充分燃烧的化学方程式相同 |
1.鲨鱼是世界上唯一不患癌症的动物,研究发现其体内含有的角鲨烯(C30H50)有抗癌作用.有关角鲨烯组成或构成的叙述正确的是( )
①角鲨烯是由碳和氢两种元素组成的
②角鲨烯是由角鲨烯分子构成的
③角鲨烯是由碳和氢两种元素构成的
④角鲨烯中含氢元素的质量分数为62.5%
⑤角鲨烯分子中碳原子和氢原子的个数比为3:5.
①角鲨烯是由碳和氢两种元素组成的
②角鲨烯是由角鲨烯分子构成的
③角鲨烯是由碳和氢两种元素构成的
④角鲨烯中含氢元素的质量分数为62.5%
⑤角鲨烯分子中碳原子和氢原子的个数比为3:5.
| A. | ①②③④⑤ | B. | ②③④⑤ | C. | ①② | D. | ①②⑤ |
2.甲同学在室温20℃时探究硝酸钾溶于水的情况,进行了如下实验: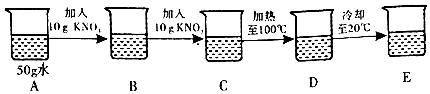
已知硝酸钾在不同温度下的溶解度如下表:
整个过程溶剂量不变,请回答问题:
(1)分析表中数据,归纳出硝酸钾的溶解度随温度变化的规律:随着温度的升高而增大.
(2)D溶液中溶剂与溶质的质量比为5:2.
(3)上述实验过程中,属于饱和溶液的是CE(填字母,下同).
(4)在B、C、D、E溶液中,溶质质量分数最小的是B.

已知硝酸钾在不同温度下的溶解度如下表:
| 温度/℃ | 10 | 20 | 60 | 100 |
| 溶解度/g | 20.9 | 31.6 | 110 | 246 |
(1)分析表中数据,归纳出硝酸钾的溶解度随温度变化的规律:随着温度的升高而增大.
(2)D溶液中溶剂与溶质的质量比为5:2.
(3)上述实验过程中,属于饱和溶液的是CE(填字母,下同).
(4)在B、C、D、E溶液中,溶质质量分数最小的是B.