题目内容
1.工业烟气脱硫就是将烟气中含有的二氧化硫除去,一种采用“双碱法”脱硫的工业流程示意图如下:(提示:SO2和NaOH的反应与CO2相似,SO2对应的酸是亚硫酸(H2SO3))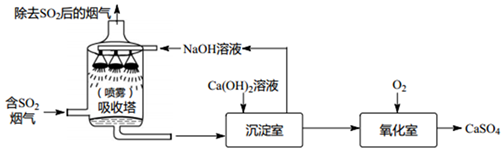
(1)如图,在吸收塔中,常把饱和的NaOH溶液喷成雾状以能充分吸收SO2,其原理是增大接触面积.反应的化学方程式为2NaOH+SO2=Na2SO3+H2O.
(2)在沉淀室中,发生了复分解反应,其中生产的不溶物质是CaSO3(填化学式).
(3)氧化室中,发生了化合反应,其化学方程式为2CaSO3+O2=2CaSO4.
(4)为了节约成本,上述流程中,可以循环利用的物质是氢氧化钠.(填名称)
分析 根据化学反应速率的影响因素解答;根据化学方程式的书写解答、根据流程图确定可以循环利用的物质.
解答 解:(1)把饱和的NaOH溶液喷成雾状能增大反应物的接触面积从而促进反应的进行,氢氧化钠能与二氧化硫反应生成亚硫酸钠和水,故填:增大接触面积;2NaOH+SO2=Na2SO3+H2O;
(2)沉淀池中氢氧化钙与亚硫酸钠反应生成了亚硫酸钙沉淀,故填:CaSO3;
(3)氧化室中亚硫酸钙和氧气反应生成了硫酸钙,故填:2CaSO3+O2=2CaSO4;
(4)根据流程图可以看出,氢氧化钠可以循环利用,故填:氢氧化钠.
点评 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力,增加了学生分析问题的思维跨度.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.从下列食品或保健品的名称看,能补充人体所必需的微量非金属元素的是( )
| A. | 高钙牛奶 | B. | 富硒康 | C. | 补锌口服液 | D. | 加铁酱油 |
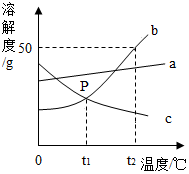 根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
 明末宋应星于崇祯十年(公元1637年)所著《天工开物》,炼锌工艺的现存文字记载:
明末宋应星于崇祯十年(公元1637年)所著《天工开物》,炼锌工艺的现存文字记载: