题目内容
2.2013年11月29日发生圆通夺命快递事件,罪魁祸首是“氟乙酸甲酯”,是一个重要的医药中间体,属于有毒化工品,具有易燃特性,刺激人的眼睛、呼吸系统和皮肤,接触不慎有致命危险,其化学式为C3H5FO2,下列关于氟乙酸甲酯说法正确的是( )| A. | 氟乙酸甲酯属于氧化物 | |
| B. | 氟乙酸甲酯中碳元素的质量分数约为39.1% | |
| C. | 氟乙酸甲酯分子是由3个碳原子、5个氢原子、1个氟原子、2个氧原子构成的 | |
| D. | 氟乙酸甲酯中碳、氢、氟、氧四种元素的原子个数比为36:5:19:32 |
分析 A、氧化物是只含有两种元素且其中一种元素是氧元素的化合物.
B、根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析判断.
C、根据氟乙酸甲酯的微观构成进行分析判断.
D、根据1个氟乙酸甲酯分子的构成进行分析判断.
解答 解:A、氟乙酸甲酯是由碳、氢、氟、氧四种元素组成的化合物,不属于氧化物,故选项说法错误.
B、氟乙酸甲酯中碳元素的质量分数约为$\frac{12×3}{12×3+1×5+19+16×2}$×100%≈39.1%,故选项说法正确.
C、氟乙酸甲酯是由氟乙酸甲酯分子构成的,1个氟乙酸甲酯分子是由3个碳原子、5个氢原子、1个氟原子、2个氧原子构成的,故选项说法错误.
D、1个氟乙酸甲酯分子是由3个碳原子、5个氢原子、1个氟原子和2个氧原子构成的,则氟乙酸甲酯中碳、氢、氟、氧原子的个数比为3:5:1:2,故选项说法错误.
故选:B.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.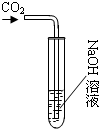 化学学习小组的同学们在探究氢氧化钠的性质时,将二氧化碳通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究.
化学学习小组的同学们在探究氢氧化钠的性质时,将二氧化碳通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究.
探究一:二氧化碳是否与氢氧化钠发生了化学反应?同学们取少量大试管中的液体于另一支试管中,滴加足量的稀盐酸,观察到有气泡冒出
证明二氧化碳与氢氧化钠发生了反应.
探究二:反应后大试管中的溶液所含溶质的成分是什么?
【提出猜想】佳佳认为溶质是Na2CO3,贝贝认为溶质是Na2CO3和NaOH
【查阅资料】CaCl2溶液呈中性
【实验验证】贝贝为了验证自己的猜想,进行了如表实验,请你补充完整.
【实验反思】同学们联想到了氢氧化钠与稀硫酸发生中和反应也观察不到明显现象,为了确定其反应是否反生,有同学设计了如下的实验方案:先用pH试纸测定氢氧化钠溶液的pH,然后向其中滴加稀硫酸,边滴边测定混合溶液的pH.请你分析上述方案中,为什么要“当测定pH小于或等于7,”才可证明发生反应了,其原因是排除因硫酸的加入,稀释氢氧化钠溶液而引起pH减小因素的干扰.
 化学学习小组的同学们在探究氢氧化钠的性质时,将二氧化碳通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究.
化学学习小组的同学们在探究氢氧化钠的性质时,将二氧化碳通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究.探究一:二氧化碳是否与氢氧化钠发生了化学反应?同学们取少量大试管中的液体于另一支试管中,滴加足量的稀盐酸,观察到有气泡冒出
证明二氧化碳与氢氧化钠发生了反应.
探究二:反应后大试管中的溶液所含溶质的成分是什么?
【提出猜想】佳佳认为溶质是Na2CO3,贝贝认为溶质是Na2CO3和NaOH
【查阅资料】CaCl2溶液呈中性
【实验验证】贝贝为了验证自己的猜想,进行了如表实验,请你补充完整.
| 实验操作 | 实验现象 | 实验结论 |
| ①取一定量大试管中的溶液于试管中,加入足量CaCl2溶液,过滤 ②向滤液滴加适量酚酞 | ①产生白色沉淀 ②溶液变红 | 贝贝的猜想成立 |
10.小丹同学在学习酸的性质时,从同一卷镁带中剪取相等的两根镁带,分别与室温下H+浓度相同的稀盐酸、稀硫酸反应.观察发现:镁带在稀盐酸中放出气泡的速率明显快于在稀硫酸中放出气泡的速率.
【查阅资料】
(1)金属与酸发生置换反应,其本质是金属单质与H+反应.
(2)生产H2速率主要取决于:①金属的表面积 ②溶液中H+浓度 ③温度等条件.
(3)H+的浓度与1L溶液中H+数目成正比.
(4)溶液中除H+外的其它离子可能会影响反应速率.
【提出问题】
①小丹同学在进行上述实验时,控制了镁带与酸反应的哪几个条件?(回答两条即可)金属的表面积,溶液中H+浓度;
②上述反应中Cl-、SO42-如何影响反应速率?
【猜想假设】
Ⅰ、Cl-促进了镁与酸的反应,SO42-对反应无影响.
Ⅱ、SO42-抑制了镁与酸的反应,Cl-对反应无影响.
Ⅲ、硫酸根抑制了镁与酸的反应,氯离子加速了镁与酸的反应.
请回答问题①,完成猜想Ⅲ.
【实验探究】
为了证明猜想,小丹设计了如下实验:
试剂B是NaCl(化学式)固体.
【结论】
结论A为钠离子、硫酸根离子对反应无影响.
【反思】
将试剂B改用HCl气体,不能达到实验目的,其原因是通入HCl气体时,形成盐酸增加了氢离子的浓度,改变了实验的条件.
【查阅资料】
(1)金属与酸发生置换反应,其本质是金属单质与H+反应.
(2)生产H2速率主要取决于:①金属的表面积 ②溶液中H+浓度 ③温度等条件.
(3)H+的浓度与1L溶液中H+数目成正比.
(4)溶液中除H+外的其它离子可能会影响反应速率.
【提出问题】
①小丹同学在进行上述实验时,控制了镁带与酸反应的哪几个条件?(回答两条即可)金属的表面积,溶液中H+浓度;
②上述反应中Cl-、SO42-如何影响反应速率?
【猜想假设】
Ⅰ、Cl-促进了镁与酸的反应,SO42-对反应无影响.
Ⅱ、SO42-抑制了镁与酸的反应,Cl-对反应无影响.
Ⅲ、硫酸根抑制了镁与酸的反应,氯离子加速了镁与酸的反应.
请回答问题①,完成猜想Ⅲ.
【实验探究】
为了证明猜想,小丹设计了如下实验:
| 实验编号 | 铝片长度 | H+浓度相同的酸 | 反应片刻后添加少量试剂 | 产生气泡的速率 | 结论 |
| A | 2cm | 5mL | Na2SO4固体 | 无明显变化 | (结论A) |
| B | 2cm | 5mL | (试剂B) | 明显变快 | Cl-对反应有促进作用 |
【结论】
结论A为钠离子、硫酸根离子对反应无影响.
【反思】
将试剂B改用HCl气体,不能达到实验目的,其原因是通入HCl气体时,形成盐酸增加了氢离子的浓度,改变了实验的条件.
 如图为甲、乙、丙三种固体物质溶解度曲线,据图回答:
如图为甲、乙、丙三种固体物质溶解度曲线,据图回答:
 在实验课上,同学们用锌和稀硫酸反应制取氢气.小明取反应后的溶液164.7g,滴入碳酸钠溶液,有气体和白色沉淀生成.加入碳酸钠溶液与生成沉淀或气体的质量关系如图.
在实验课上,同学们用锌和稀硫酸反应制取氢气.小明取反应后的溶液164.7g,滴入碳酸钠溶液,有气体和白色沉淀生成.加入碳酸钠溶液与生成沉淀或气体的质量关系如图.